 |
|
| Appunti universita |
|
 |
|
| Appunti universita |
|
| Visite: 4620 | Gradito: |
Leggi anche appunti:ScreeningScreening gli screening oncologici sono interventi di sanita pubblica Patologia respiratoria - bambinoPATOLOGIA RESPIRATORIA - BAMBINO Verranno trattate le principali patologie respiratorie PneumococchiPNEUMOCOCCHI · Pneumococco o streptococco pneumoniae · Cocchi, |
 |
 |
CARDIOLOGIA PEDIATRICA
Cardiopatie congenite
Dati epidemiologici: Le cardiopatie neonatali si verificano nei primissimi mesi di vita e spesso portano alla morte del paziente.
![]()
 Ogni anno in Italia nascono circa 4000-4500
bambini con cardiopatia congenita. La diagnosi viene posta entro la prima
settimana di vita nel 45% dei pz. ed entro il primo mese di vita nel 55%.
Ogni anno in Italia nascono circa 4000-4500
bambini con cardiopatia congenita. La diagnosi viene posta entro la prima
settimana di vita nel 45% dei pz. ed entro il primo mese di vita nel 55%.
Grazie ai progressi della chirurgia palliativa e correttiva, il numero dei bambini con CHD che sopravvivono fino all'età adulta è aumentato in modo significativo; ciononostante le CHD rimangono la causa principale di morte nei bambini con malformazioni congenite.
Su 4390 pazienti affetti da una cardiopatia congenita 800 (il 18%) muoiono, di questi l'80% muore nella prima settimana. Il decesso nel 43% avviene nel post-operatorio, nel 47% durante il decorso naturale della malattia mentre nel restante 10% non era stata fatta una diagnosi clinica definita. Bisogna considerare che esistono anche patologie cardiache pediatriche minori meno gravi.
Eziologia
Ipotesi multifattoriale: veniva in passato evocata per la quasi totalità di queste malformazioni;
Cause puramente genetiche: Gli studi epidemiologici, clinici, citogenetici e di biologia molecolare hanno permesso di definire l'origine precisa della gran parte delle cardiopatie associate a sindromi ed una intensa attività di ricerca è attualmente dedicata ai difetti cardiaci isolati. Le correlazioni genotipo-fenotipo nell'uomo e la sperimentazione genetica sugli animali stanno iniziando a chiarire i meccanismi patogenetici, che dalla anomalia genetica portano al difetto anatomico. Le prospettive di terapia genica sono comunque assai lontane in questo campo e le possibilità di prevenzione sono attualmente legate ad una accurata consulenza genetica familiare ed agli interessanti risultati del trattamento materno con acido folico;
I fattori ambientali non genetici: incidono maggiormente nei tratti complessi mentre risultano di minore importanza se sono presenti singoli geni o geni multipli.
E' importante procedere ad un'attenta anamnesi in un neonato affetto da cardiopatia congenita. Bisogna valutare anche la presenza di patologie genetiche nei familiari. Bisogna mettere a proprio agio i familiari del bambino, valutare tutte le indagini che sono state fatte al bambino e ordinarle in ordine cronologico in modo da ipotizzare il quadro patologico presente.
La causa della maggior parte delle cardiopatie congenite è sconosciuta. In passato si riteneva che nella maggior parte dei casi le cardiopatie congenite fossero multifattoriali e risultassero dalla combinazione di una predisposizione genetica e di uno stimolo ambientale.
Una piccola percentuale di lesioni cardiache congenite è correlata ad anomalie cromosomiche, in particolare trisomia 21 (Il 50% circa degli affetti da sindrome di Down ha una cardiopatia congenita tra le quali la più frequente è il difetto tipo ostium primum, talora un canale completo (valvola atrioventricolare comune tra cuore destro e sinistro), trisomia 13, trisomia 18 e SindromeTurner.
L'analisi con tecnica FISH (Fluorescence In Situ Hybridization) permette ai medici un rapido screening dei casi sospetti, una volta che sia stata identificata una specifica anomalia cromosomica.
Anamnesi
Presenza di cardiopatie congenite o sindromi genetiche nei familiari;
Eventi patologici intercorsi durante i primi 3 mesi di gestazione (infezioni virali, assunzione di farmaci potenzialmente teratogeni, droghe, alcool, esposizione a radiazioni ionizzanti, malattia cronica della madre).
Sintomi più frequentemente riferiti dai genitori:
Cianosi a riposo o durante sforzi più o meno intensi;
Dispnea (difficoltà respiratoria);
Difficoltà nell'alimentazione;
Scarso accrescimento;
frequenti infezione broncopolmonari;
facile affaticabilità;
tachicardia anche a riposo.
Questa sintomatologia può andare in diagnosi differenziale con la fibrosi cistica, il bambino affetto da FC cresce poco fin dalla nascita.
Esame clinico: Si esegue in un ambiente confortevole, caldo, tranquillo; possibilmente si fa spogliare completamente il bambino. Possiamo valutare la presenza di cianosi periferica e lo stato di nutrizione del paziente.
L'esame clinico si compone delle 4 fasi : Ispezione, Palpazione, Percussione, Auscultazione.
All'ispezione valutiamo:
Dismorfismi;
Stato di nutrizione;
Dispnea;
Cianosi;
Edemi;
Bozza precordiale (orienta verso una cardiopatia ad esordio precoce);
Itto visibile;
Turgore giugulari.
Dismorfismi: Per quanto riguarda i dismorfismi si deve porre attenzione al fenotipo, agli aspetti esteriori che indicano la presenza di sindromi malformative frequentemente associate a cardiopatia congenita come:
Sindrome di Down;
Sindrome di Turner;
Sindrome di Williams;
Sindrome di Marfan;
Sindrome di Holt-Oram;
Sindrome di DiGeorge;
Sindrome di Noonan/Leopard;
 Sindrome di Ellis van Creveld.
Sindrome di Ellis van Creveld.
La sindrome di Down presenta un'incidenza di 1:750 e l'aspettativa media di vita è di circa 50 anni. E' associata a compromissione cognitiva, dimorfismi facciali, difetti cardiaci congeniti (difetti a carico del setto interventricolare, difetti del setto atrioventricolare, del septum secundum atriale, pervietà del dotto arterioso, tetralogia di Fallot), anomalie GI, leucemia, malattia di Alzheimer, disfunzione immunitaria, ipotiroidismo, DM, problemi della vista e dell'udito.
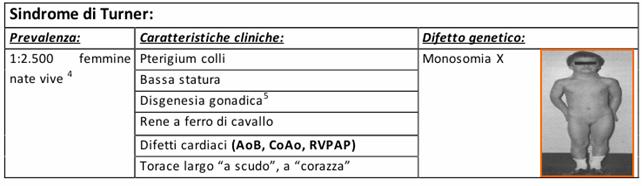
I pazienti affetti da sindrome di Turner presentano bassa statura, orecchie sporgenti, collo palmato ed edema delle mani e dei piedi anche se molti soggetti sono fenotipicamente normali. Sono presenti anche difetti cardiaci congeniti e anomalie strutturali renali. I difetti cardiaci più frequenti sono:le valvole aortiche bicuspidi, la coartazione aortica, la stenosi aortica e il prolasso della valvola mitralica. Le gonadi sono costituite da strie di tessuto fibroso, si riscontra amenorrea primaria e assenza di caratteri sessuali secondari.
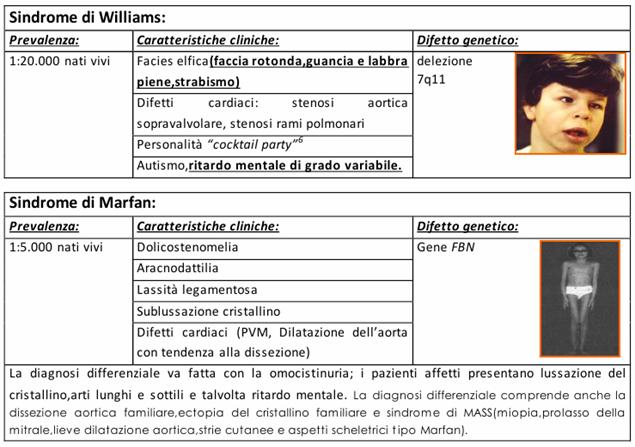
La sindrome di Marfan, malattia autosomica dominante, presenta un pattern di malformazioni tipicamente cardiovascolari, scheletriche e oculari. La sindrome di Marfan neonatale si presenta con ipotonia, aracnodattilia, lassità legamentosa, lussazioni e retrazioni in flessione; il viso è allungato, la cute è lassa, le orecchie sono talora grandi e pieghevoli. L'esame oculare può mostrare lussazione del cristallino e l'esame cardiologico spesso rileva soffi da prolasso mitralico con o da insufficienza aortica. Una dilatazione della radice aortica può essere documentata con l'ecocardiografia. I bambini più grandi presentano sclere blu, miopia e lassità del legamento sospensore con iridocinesi. L'esame dell'apparato muscolo scheletrico evidenzia arti lunghi e sottili e un rapporto tronco e arto superiore esagerato per l'altezza. Il segmento inferiore è maggiore rispetto al superiore. I difetti cardiovascolari progressivi contribuiscono alla morbilità della sindrome di Marfan.
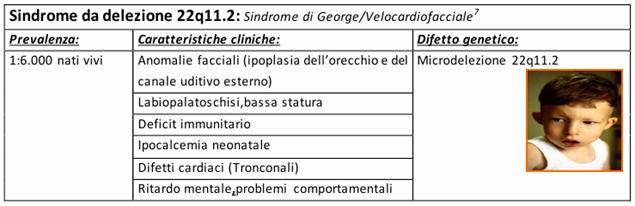
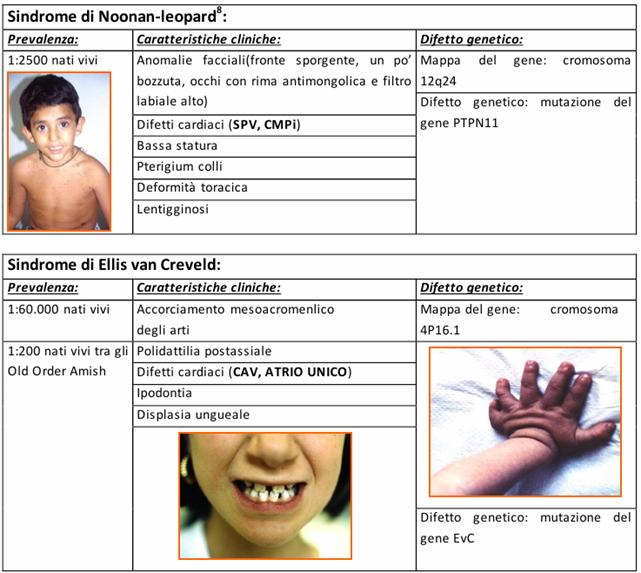
La sindrome di Ellis von-Creveld o displasia condroectodermica (malattia AR) è una displasia scheletrica ed ectodermica. La displasia scheletrica si presenta arti corti specialmente nei segmenti distali e medi, polidattilia post-assiale delle mani e talvolta dei piedi. La displasia ectodermica si presenta con displasia delle unghie e anomalie dentali. Sono presenti anche il difetto del setto interatriale e altre cardiopatie congenite.
Crescita e stato di nutrizione
Possono essere normali;
Compromessi nei bambini con insufficienza cardiaca cronica;
Statura: di solito è conservata (diminuisce nelle forme gravi);
Peso: crescita ponderale rallentata: minor introito calorico per difficoltà nell'alimentazione;
maggior dispendio energetico a causa dello sforzo respiratorio (dispnea).
Dispnea
Aumento della frequenza degli atti del respiro (tachipnea). La FR va valutata durante il sonno;
Rientramenti inspiratori al giugulo, agli spazi intercostali e all'epigastrio;
Alitamento delle ali del naso.
Questi sintomi sono un'indicazione al ricovero.
![]()
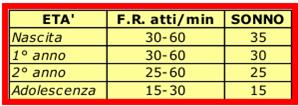 Le cause di dispnea più frequenti nel bambino
sono:
Le cause di dispnea più frequenti nel bambino
sono:
Iperafflusso polmonare da cardiopatie congenite con shunt sn-dx;
Scompenso cardiaco congestizio (incapacità della pompa cardiaca a mantenere un'adeguata circolazione);
Malattie polmonari.
Colorito cute e mucose: Pallore e/o marezzatura (con cute sudata ed estremità fredde) a causa della bassa gittata determinata da insufficienza cardiaca.
![]()
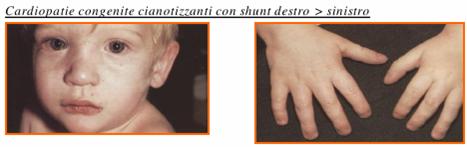 Cianosi: Colorazione bluastra della cute e delle mucose prodotta da
aumento della concentrazione assoluta di Hb ridotta nei capillari (> 5 g/dl)
o dalla presenza di composti anomali della Hb.
Cianosi: Colorazione bluastra della cute e delle mucose prodotta da
aumento della concentrazione assoluta di Hb ridotta nei capillari (> 5 g/dl)
o dalla presenza di composti anomali della Hb.
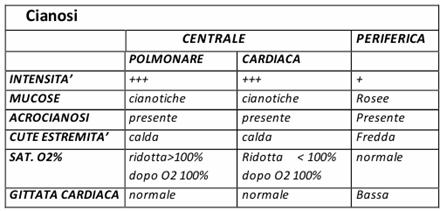
Quando parliamo di cianosi possiamo distinguere una cianosi di origine centrale e una di origine periferica.
Una cianosi si definisce centrale quando vi è una ridotta saturazione arteriosa sistemica in O2. A sua volta una cianosi centrale può essere di origine polmonare o cardiaca. Quando è di origine polmonare può essere determinata da:
Ridotta ventilazione;
Alterazione scambi alveolari;
Alterato rapporto ventilazione/perfusione
Una cianosi di origine cardiaca è dovuta a:
Shunt Dx>Sn;
Ipoafflusso polmonare.
Si parla, invece, di cianosi periferica quando vi è un'aumentata estrazione di O2 da parte dei tessuti. Può essere determinata da:
Ridotta perfusione;
Rallentato circolo;
Ostacolato scarico venoso distrettuale.
Un tipo di cianosi particolare è quella determinata da pigmento emoglobinico anomalo. In questo gruppo distinguiamo:
![]()
 Metaemoglobinemie, che può essere Congenita o
Acquisita; Scompare con sostanze riducenti. Esistono alcuni farmaci come il
farmaco antilebbra che rafforzano i meccanismi di preservazione della vita
delle piastrine. In pazienti affetti da porpora trombocitopenia idiopatica che
non risponde bene alla terapia con steroidi o Ig e.v. può essere utilizzato
questo farmaco contro la lebbra che riduce la dose di cortisone da
somministrare. Inoltre crea dei ponti tra le varie globine precipitando così
sottoforma di mataemoglobinemia;
Metaemoglobinemie, che può essere Congenita o
Acquisita; Scompare con sostanze riducenti. Esistono alcuni farmaci come il
farmaco antilebbra che rafforzano i meccanismi di preservazione della vita
delle piastrine. In pazienti affetti da porpora trombocitopenia idiopatica che
non risponde bene alla terapia con steroidi o Ig e.v. può essere utilizzato
questo farmaco contro la lebbra che riduce la dose di cortisone da
somministrare. Inoltre crea dei ponti tra le varie globine precipitando così
sottoforma di mataemoglobinemia;
Solfoemoglobinemia: Resiste agli agenti riducenti;
Carbossiemoglobinemia: Intossicazione monossido di Carbonio.
In corso di ipossia all'ispezione ritroviamo il segno del clubbing digitale, che consiste in un ispessimento delle falangi terminali delle dita associato allo sviluppo di unghie iperconvesse (dita a bacchetta di tamburo e unghie a vetrino d'orologio).
I meccanismi fisiopatologici alla base di tale fenomeno sono:
Aumento del numero dei capillari (fenomeno neo angiogenetico);
Aumento del flusso ematico attraverso microaneurismi arterovenosi;
Iperplasia connettivale.
Pazienti con MICI o con FC del pancreas possono presentare unghia a vetrino d'orologio ma senza la cianosi.
Edema: Per edema si intende un'imbibizione del tessuto sottocutaneo dovuta ad una ritenzione idro-salina. Nel bambino grandicello si sviluppa più frequentemente un edema malleollare, mentre se il bambino è allettato si avrà più facilmente un edema sacrale. Nel lattante si può osservare un edema palpebrale. E' importante nella pratica clinica in caso di edema pesare ogni giorno il bambino per vedere se l'edema si riassorbe.
Bozza precordiale: Si può ritrovare nei lattanti con cardiomegalia.
Itto visibile: Segno di cardiomegalia. Possiamo ritrovarlo a livello dell'epigastrio e ci indicherà una dilatazione del VD, oppure lo ritroviamo verso l'ascella e sarà indice di dilatazione VS.
Turgore giugulari: Sovraccarico atriale destro.
Reticoli venosi superficiali: Segno di aumentata pressione venosa nel distretto inferiore.
Palpazione: Andiamo a ritrovare alcuni segni come:
Itto della punta;
Fremito;
Epatomegalia;
Polsi periferici;
Riempimento capillare.
Itto della punta: Nel neonato e nel lattante, rispetto all'adulto, il cuore è più orizzontale per cui l'itto lo si ritrova al IV SIS (spazio intercostale sinistro), esternamente all'emiclaveare. Nel Bambino e nell'adulto, invece, l'itto si ritrova al IV-V SIS all'interno dell'emiclaveare.
Fremito: Si intende la vibrazione trasmessa in presenza di un soffio ad alta intensità, equivalente palpatorio del soffio.
Epatomegalia: Nei lattanti normali il margine epatico può arrivare fino a 2-2.5 cm al di sotto dell'arcata costale destra; nel bambino più grande fino a 1 cm.
Polsi arteriosi
Polsi radiali, femorali, pedidii e carotidei su entrambi i lati;
Polsi femorali assenti o ritardati rispetto ai polsi radiali sono un sospetto di coartazione aortica.
Riempimento capillare: Valuta l'efficienza della circolazione cutanea. Se > 3 sec: ridotta perfusione periferica (per problemi cardiaci o per una grave disidratazione).
Percussione: Si valuta l'Aia cardiaca.
Ascoltazione
Ritmo e frequenza;
Rilevazione Pressione Arteriosa;
Toni cardiaci;
Soffi cardiaci.
Ritmo: Nel Neonato e nel lattante l'attività cardiaca è, generalmente, ritmica, tranne che nel sonno in cui sono frequenti brevi periodi di bradicardia. Nei bambini e negli adolescenti, invece, si ha un'aritmia respiratoria più o meno marcata, che talvolta simula l'extrasistolia.
Frequenza cardiaca: Dipende dall'età. La frequenza cardiaca va valutata durante il sonno. Un neonato che presenta una FC superiore a 160 batt/minuto molto probabilmente ha un problema cardiaco. Anche la pressione arteriosa varia dipende dall'età. Si valutano i percentili in base all'età del bambino. Bisogna misurare la P.A. ai 4 arti con apparecchi elettronici e bracciali adatti ( 2/3 del braccio).
Toni cardiaci: Il I Tono corrisponde alla chiusura delle valvole atrioventricolari e raramente lo si ritrova sdoppiato nei bambini. Il II tono corrisponde alla chiusura delle valvole semilunari, e il grado di sdoppiamento può variare con gli atti del respiro. Il III tono è dovuto al riempimento ventricolare rapido, può essere presente nei bambini sani, è patologico negli adulti. Il IV tono è dovuto alla contrazione atriale ed è sempre patologico.
Soffio: Quando il flusso ematico da laminare diviene turbolento genera un soffio cardiaco. Quando si valuta un soffio bisogna considerare il focolaio di auscultazione cardiaca sul quale ci si trova, la fase del ciclo e l'intensità, valutata con la scala di Levine.
Sulla base del ciclo cardiaco distinguiamo:
Soffi sistolici: protosistolico; olosistolico; mesosistolico; telesistolico;
Soffi diastolici: protodiastolico; mesodiastolico; telediastolico;
Soffio sisto-diastolico: continuo.
L'intensità del soffio viene classificata in gradi secondo la scala di Levine:
1/6: appena udibile;
2/6: debole ma facilmente udibile;
3/6: moderatamente forte, non accompagnato da fremito;
4/6: forte, accompagnato da fremito;
5/6: udibile con il fonendoscopio che sfiora il torace;
6/6: udibile con il fonendoscopio staccato dal torace.
I soffi cardiaci possono essere classificati in soffi organici, in cui si ritrova un'alterazione anatomica o cause extracardiache (funzionale), e in soffi innocenti, udibili in assenza di alterazioni cardiache o extracardiache sia anatomiche che funzionali.
Caratteri costanti di soffi innocenti sono:
Sono praticamente sempre sistolici;
Sono di breve durata, proto o protomesosistolici;
Spesso hanno caratteristiche di eiezione;
Sono dolci e di timbro musicale;
Sono di debole intensità (1 - 2/6);
Sono isolati, non si apprezzano modificazioni dei toni o toni aggiunti patologici.
Fino ai 10-11 anni possono essere presenti soffi innocenti, di solito tendono a normalizzarsi intorno ai 5-7 anni.
Diagnostica Strumentale
Rx del torace;
Ecg;
Ecocardiografia color doppler;
Risonanza magnetico nucleare;
Cateterismo cardiaco (viene fatto sempre di meno, importante nel pre-operatorio);
Angiocardiografia;
Ecg holter(per alterazione della frequenza cardiaca);
Studio elettrofisiologico;
Monitoraggio della pressione arteriosa.
Rx torace: Fornisce informazioni utili per visualizzare:
Flusso polmonare;
Ombra cardiaca;
Posizione dei visceri e del cuore;
Eventuali patologie polmonari associate.
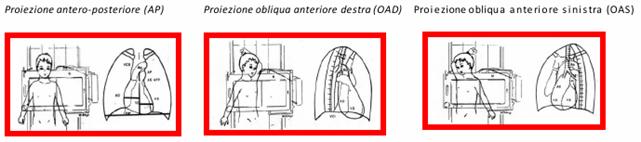
Figura : Rx del torace e proiezioni.
La Rx del torace è un esame poco costoso, non richiede personale specializzato per eseguirlo. Una radiografia standard del torace non espone il paziente ad una alta dose di radiazione. Un altro parametro che viene analizzato è l'indice cardiaco.
Elettrocardiogramma
Disturbi del ritmo;
Ipertrofie atriali;
Ipertrofie ventricolari;
Sovraccarichi pressori;
Alterazioni della ripolarizzazione ventricolare (su base ischemica o per squilibri elettrolitici).
L'elettrocardiografo è lo stesso che viene usato nell'adulto mentre vengono utilizzati elettrodi differenti: si tratta di sensori posizionati su un piccolo adesivo monouso che permette di evitare la diffusione di infezioni.
Differenze con l'adulto:
Ipertrofia ventricolare destra per ipervoltaggio nelle derivazioni destre;
Deviazione assiale destra: R in aVR;
R/S > 1 su precordiali destre, R è più alta di S sulle precordiali destre;
T + su precordiali destre;
T - dopo 36 ore di vita.
Ecocardiografia
Mono e Bidimensionale;
Doppler PW - CW - Color;
Tridimensionale.
Bidimensionale: diagnosi della quasi totalità delle cardiopatie congenite tramite visualizzazione delle strutture cardiache e della cinesi.
PW-CW: velocità del flusso del sangue attraverso strutture cardiache e grossi vasi (per stimare i gradienti).
Color Doppler: valuta in tempo reale flussi ematici all'interno del cuore e dei grossi vasi.
Cateterismo cardiaca: Procedura sia Diagnostica che interventistica. Il cateterismo diagnostico permette di valutare: parametri emodinamici, pressioni e saturazioni nelle diverse camere cardiache e nei grossi vasi. Con metodiche angiocardiografia si possono visualizzare camere cardiache, grossi vasi ed arterie coronarie.
Il cateterismo interventistico permette diverse procedure come: Atriosettostomia, Valvuloplastica; Applicazione dispositivi occlusivi (pda, dia, div, fistole av); Coronarografia in paziente con malattia di Kawasaki e grave compromissione coronarica. La malattia di Kawasaki è caratterizzata da febbre, alterazioni delle mucose, vascolopatia immuno-allergica che coinvolge anche il cuore; sono presenti alterazioni coronariche che determinano alterazioni infartuali. Il paziente deve essere trattato con l'aspirina, il trattamento è salva-vita.
Classificazione delle cardiopatie congenite
 Le anomalie strutturali delle cardiopatie
congenite possono essere schematizzati come segue:
Le anomalie strutturali delle cardiopatie
congenite possono essere schematizzati come segue:
Difetti di settazione;
Anomalie di connessione: delle vene agli atri, degli atri ai ventricoli e dei ventricoli alle arterie;
Ostruzione all'efflusso (polmonare o aortico) o all'afflusso (destro o sinistro);
Associazioni delle precedenti;
Anomalie di situs viscero-atriale: malposizioni cardiache, spesso associate alle precedenti.
Due delle molteplici classificazioni di queste patologie sono di utilità clinica e didattica. La classificazione clinica (detta anche 'classica') distingue le cardiopatie in base alla presenza di cianosi e presenza di scompenso in:
![]() Cianogene;
Cianogene;
Non cianogene;
Con scompenso;
Senza scompenso.
La classificazione fisiopatologica si focalizza sul flusso polmonare e divide le cardiopatie in:
Con iperafflusso polmonare (difetti settali);
Con ipoafflusso polmonare (ostruzioni all'efflusso associate a difetti settali, sono cianogene);
Con normoflusso polmonare (coartazione, stenosi aortica o polmonare isolate).
Difetto interventricolare (DIV)
I difetti del setto interventricolare rappresentano circa il 33% delle CHD. La maggioranza dei DIV sono piccoli-medi e questi si chiudono spontaneamente grazie alla crescita muscolare miocardica.
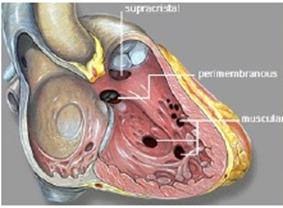 Possono essere classificati in base alla sede
in:
Possono essere classificati in base alla sede
in:
difetti del setto muscolare trasecolare;
difetti del setto membranoso, detti anche perimembranosi, localizzati in vicinanza degli osti arteriosi, vicino agli atri difetti del setto muscolare infundibolare (rari).
Invece la classificazione fisiopatologica li suddivide in:
![]() DIV piccolo o restrittivo: shunt SN>DX
piccolo; pressione nel ventricolo destro normale; QP/QS<1.5 (QP = portata
polmonare; QS = portata sistemica);
DIV piccolo o restrittivo: shunt SN>DX
piccolo; pressione nel ventricolo destro normale; QP/QS<1.5 (QP = portata
polmonare; QS = portata sistemica);
DIV moderato: shunt moderato con 1,5 < QP/QS <2,2;
DIV ampio o non restrittivo: non offre resistenze al flusso, la pressione del ventricolo destro risulta essere uguale a quella del ventricolo sinistro; QP/QS >2,2.
Segni e Sintomi: DIV piccoli sono asintomatici. DIV grandi causano scompenso cardiaco già dal 1° mese che si manifesta con ritardo di crescita, sudorazione durante i pasti e dispnea; segue un periodo di apparente benessere ed infine si sviluppa la Sindrome di Eisenmenger. Tanto più ampio è il difetto tanto più grande è l'entità dello shunt e quindi tanto più equilibrate sono le pressioni nei due ventricoli. L'iperafflusso polmonare derivante provoca a lungo andare l'ipertensione polmonare e quindi l'inversione dello shunt che sarà da destra a sinistra con la comparsa di cianosi. Questa condizione va sotto il nome di sindrome di Eisenmenger.
All' EO: un DIV restrittivo genera, dopo la nascita, quando si riducono le resistenze vascolari polmonari, un soffio olosistolico al mesocardio; un DIV ampio: permetterà l'eguagliarsi delle pressioni ventricolari destre e sinistre, non generando in tal modo alcun soffio, ma potendo causare epatomegalia da scompenso cardiaco congestizio; un secondo tono unico e accentuato può indicare ipertensione polmonare tipica della S. di Eisenmenger.
L'ECG documenta l'ipertrofia destra adattativa (ampi complessi QRS in V1-4) o ipertrofia bilaterale. Il quadro radiologico è quello di iperafflusso polmonare e sono frequenti aneurismi dei vasi polmonari nell'adulto.
L'ecocardiografia è l'esame diagnostico per eccellenza e permette di valutare: sede, dimensione, Jet, gradienti pressori e di stimare indirettamente la pressione arteriosa polmonare sistolica.
Un cateterismo cardiaco è indicato dopo il 1° anno di vita se si sospetta patologia vascolare polmonare.
Terapia
medica: diuretici per migliorare la sintomatologia;
percutanea: chiusura con device dedicato;
chirurgica: con sutura diretta o patch.
Indicazioni all'intervento:
DIV piccolo, sintomatico che non risponde a terapia medica;
DIV moderato/ampio, sintomatico, QP/QS >1,5;
Pressione arteriosa sistolica polmonare >50mmHg.
Difetti interatriali (DIA)
I difetti del setto interatriale rappresentano circa il 7,5% delle CHD.
![]()
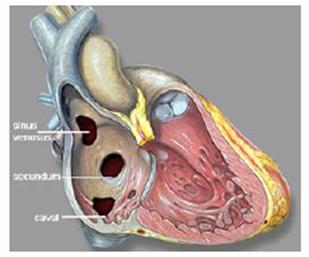 Classificazione
Classificazione
Difetto della fossa ovale (ostium secundum) è il più frequente, manca il pavimento della fossa ovale;
Difetto atrioventricolare parziale (tipo ostium primum);
Difetto del seno venoso, localizzato al di sotto dello sbocco della VCS, si associa a ritorni anomali delle vene polmonari dx;
Difetto cavale inferiore, localizzato a livello della VCI.
Fisiopatologia: Shunt sin-dx la cui entità dipende dalle dimensioni del difetto e dalle rispettive pressioni di riempimento diastolico dei due ventricoli. La chiusura spontanea può verificarsi nel primo anno di vita. Shunt significativo/ampio determina sovraccarico di volume delle sezioni Dx con dilatazione.
Sintomi: solitamente ASINTOMATICI (raramente: ritardo dell'accrescimento, scompenso cardiaco).
EO: Soffio sistolico eiettivo sulla polmonare; II tono sdoppiato "fisso".
ECG: BBDx incompleto (rSR' in V1). ETT, ETE13 : esami diagnostici!
Scelte terapeutiche
Chiusura percutanea con Device dedicato (solo per i DIA ostium secundum);
Chiusura chirurgica con sutura diretta o patch di pericardio o sintetico.
Indicazione all'intervento:
QP/QS<1,5: NON richiede correzione;
QP/QS>1,5 o DIA con sovraccarico di volume ventricolare destro: Richiede correzione.
Dotto arterioso pervio (Patent Doctus Arteriousus - PDA)
Rappresentano circa il 7% delle CHD. Hanno un'incidenza maggiore nei prematuri. La chiusura spontanea si verifica in circa il 90% entro i primi 2 mesi di vita e nel 99% entro il primo anno di vita.
Classificazione
Silente: PDA con minimo shunt;
Piccolo: soffio continuo; QP/QS < 1,5;
Moderato: soffio continuo; 1,5 < QP/QS < 2,2;
Grande: QP/QS > 2,2.
Caratteristiche clinico- fisiopatologiche
![]()
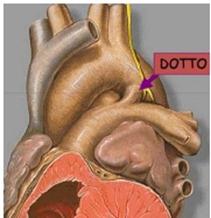 PDA silenti: asintomatico, no alterazioni
emodinamiche;
PDA silenti: asintomatico, no alterazioni
emodinamiche;
PDA piccoli: asintomatico, no alterazioni emodinamiche, piccolo shunt, predisposizione ad endoarterite;
PDA moderati: alterazioni emodinamiche: sovraccarico di volume dell'atrio sinistro (con Fibrillazione Atriale e palpitazioni) e del ventricolo sinistro (disfunzione ventricolare sin con dispnea);
PDA grande: sovraccarico di volume ventricolare sin con progressivo incremento PAP e Sindrome di Eisenmenger.
EO: Soffio continuo in sottoclaveare sinistra.
ECG: Normale o ipertrofia biventricolare.
ETT: Jet che indica lo shunt sin-dx dall'Aorta discendente al ramo polmonare sin.
Indicazione all'intervento: Neonati prematuri con shunt significativo ed alterazioni emodinamiche:
Ibuprofene o indometacina per inibire la sintesi di PGE;
Legatura chirurgica. Bambini e Adulti con PDA moderato/grande: Chiusura del PDA.
Scelte terapeutiche per Chiusura del PDA:
Chiusura percutanea con Device dedicato;
Chiusura chirurgica con legatura e/o sezione del dotto.
Coartazione dell'aorta
Restringimento localizzato in corrispondenza della parete aortica postero-laterale spesso a valle dell'origine dell'arteria succlavia sin. Rappresenta circa il 6 % delle CHD. Molto frequente nella Sindrome di Turner. È associata a bicuspidia aortica in più del 70% dei pz.
Classificazione clinico-fisiopatologica
Ostruzione grave: insufficienza ventricolare sinistra e ipoperfusione sistemica (soprattutto renale) già in età neonatale;
Ostruzione moderata: ipertrofia ventricolare concentrica in età adulta, ipertensione del distretto superiore, circoli collaterali (polsi intercostali).
Segni e Sintomi: spesso asintomatica, alcuni bambini presentano claudicatio sotto sforzo. Il segno classico è una disparità di pressione sanguigna tra arto superiore ed inferiore con iposfigmia dei polsi femorali.
EO: Soffio sistolico lungo il margine sternale sinistro (III-IV spazio intercostale).
Diagnostica strumentale: ETT, RMN (gold standard).
Indicazione all'intervento: Coartazione aortica significativa.
Scelte terapeutiche:
Dilatazione con catetere a palloncino nella sede della coartazione;
Impianto di stent nella sede della coartazione;
Aortoplastica chirurgica.
Stenosi aortica congenita
Classificazione
Valvolare: 75%, lembi ispessiti e commissure fuse;
Sottovalvolare/subaortica: cercine fibromuscolare al di sotto della valvola, possibile rapido aggravamento, spesso diagnosi tardiva;
Sopravalvolare: rara, sporadica, familiare o associata alla sindrome di Williams.
Segni e Sintomi: sintomatologia dipendente dall'entità dell'ostruzione. Neonato: severa bassa gittata (cianosi periferica, polsi iposfigmici, oligurico, tachipnea). Bambino più grande: astenia, angina e sincope.
EO: soffio al II SID e marginosternale sx. Diagnostica strumentale: ETT.
Terapia
per le forme sottovalvolari a diaframma la terapia elettiva è l'escissione chirurgica della membrana;
per le forme valvolari la terapia di scelta è la valvuloplastica con catetere a pallone eseguita per via percutanea;
le forme sopravalvolari vengono trattate chirurgicamente mediante l'inserimento di un patch di allargamento con morfologia a Y rovesciata.
L'indicazione all'intervento viene posta in presenza di gradienti medi al Doppler > 50 mmHg.
Stenosi Polmonare
È una cardiopatia caratterizzata da un'ostruzione all'efflusso ventricolare destro che può essere localizzata a livello sottovalvolare (infundibolare), valvolare (la più frequente) o sopravalvolare.
La stenosi della valvola polmonare rappresenta, come difetto isolato, circa il 5-10% di tutte le cardiopatie congenite e più frequentemente si associa ad altri difetti cardiaci (es. tetralogia di Fallot). Non di rado è presente nella sindrome di Noonan o nella sindrome di Turner.
Clinica: I caratteri clinici della stenosi polmonare dipendono dall'entità della stenosi:
le stenosi lievi-moderate, se la valvola tricuspide è ben continente e non vi sono difetti di conduzione, sono in genere asintomatiche;
le stenosi gravi danno luogo alla comparsa dei sintomi quali dispnea, astenia e facile affaticabilità;
la stenosi critica (forma valvolare critica del neonato), cardiopatia dotto-dipendente, è caratterizzata da ipossia e cianosi.
Diagnosi
Segni obiettivi: Click sistolico di apertura della valvola polmonare (auscultabile sul focolaio della polmonare) la cui precocità è direttamente proporzionale al grado di stenosi;
Soffio sistolico polmonare a diamante, aspro e rude. L'acme dell'intensità (in genere mesosistolico) ritarda in modo direttamente proporzionale al grado di stenosi;
II tono marcatamente sdoppiato;
In stenosi gravi: IV tono.
L'ECG può essere normale nelle forme lievi, mentre nelle forme più gravi possono comparire P polmonari (da sovraccarico atriale destro) e segni di ipertrofia ventricolare destra.
Anche l'RX può essere del tutto normale nelle forme lievi, mentre nelle forme più gravi può mostrare ipovascolarizzazione polmonare, prominenza del secondo arco sinistro (per dilatazione post-stenotica dell'arteria polmonare) e ingrandimento ventricolare destro.
L'ecocardiografia consente una approfondita analisi morfo-funzionale della valvola polmonare e dei flussi trans-valvolari (con il color-doppler).
Trattamento: Il trattamento può essere con valvuloplastica percutanea o un intervento chirurgico (valvulotomia o resezione chirurgica del tessuto muscolare infundibolare ipertrofico in caso di stenosi sottovalvolare).
Tetralogia di Fallot
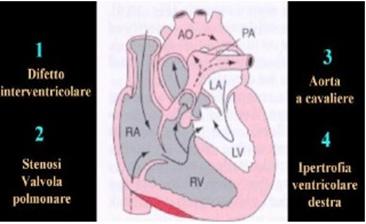 È una cardiopatia cianogena caratterizzata da
difetto interventricolare, stenosi della valvola polmonare, aorta a cavaliere
(del DIV) e ipertrofia ventricolare destra (che consegue alla stenosi
polmonare).
È una cardiopatia cianogena caratterizzata da
difetto interventricolare, stenosi della valvola polmonare, aorta a cavaliere
(del DIV) e ipertrofia ventricolare destra (che consegue alla stenosi
polmonare).
La tetralogia di Fallot rappresenta circa il 5-7% delle cardiopatie congenite e tra le cardiopatie cianotiche è la più frequente.
![]() Clinica: Le manifestazioni cliniche dipendono dalla direzione dello
shunt interventricolare che quindi configura due quadri:
Clinica: Le manifestazioni cliniche dipendono dalla direzione dello
shunt interventricolare che quindi configura due quadri:
il "Fallot classico", in cui vi è uno shunt destro>sinistro. Si ha quindi cianosi, aumentata frequenza respiratoria e affaticabilità. I sintomi compaiono tanto precocemente quanto più grave è la stenosi;
il "Fallot roseo", in cui vi è uno shunt sinistro>destro. Il quadro clinico è simile a quello rilevabile in caso di difetto interventricolare.
Poiché la direzione dello shunt è determinata dalla differenza di pressione che c'è tra i due ventricoli e poiché questa differenza è determinata dal grado di stenosi polmonare, in ultima analisi le manifestazioni cliniche dipendono dal grado di stenosi polmonare:
se la stenosi polmonare è in grado di determinare uno shunt destro>sinistro si ha il Fallot classico;
se la stenosi polmonare non determina uno shunt destro>sinistro e si ha quindi uno shunt sinistro>destro si ha il Fallot roseo.
Cyanotic (o Hypercyanotic) spell (crisi di cianosi marcata): Complicanza determinata da eventi che inducono una brusca elevazione delle resistenze polmonari o diminuzione di quelle sistemiche quali pianto, fatica, attività fisica.
Diagnosi: I reperti obiettivi ed ECGgrafici sono simili a quelli della stenosi polmonare per il Fallot classico e a quelli del DIV per il Fallot roseo. All'RX torace si ritrova il tipico aspetto di punta sollevata e arrotondata ("a scarpa") con secondo arco sinistro concavo e campi polmonari variabilmente ipoperfusi. L'ECO mostra la tipica l'immagine di cavalcamento dell'aorta sul setto interventricolare.
Trattamento: Nella tetralogia di Fallot severa l'approccio terapeutico immediato consiste nell'assicurare la pervietà del dotto di Botallo mediante prostaglandine. In seguito si procede alla correzione chirurgica radicale che può essere primaria, o può essere preceduta da interventi palliativi. In genere precocemente si effettua un intervento palliativo (Blalock- Taussig Shunt modificato ) e poi, verso i 6-18 mesi, si effettua l'intervento radicale con chiusura del DIV e correzione della stenosi.
Trasposizione delle grosse arterie
È una cardiopatia cianogena in cui l'aorta origina dal ventricolo destro e l'arteria polmonare dal ventricolo sinistro (discordanza ventricolo-arteriosa).
![]()
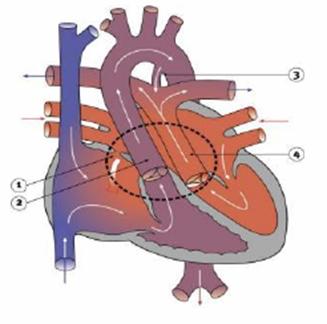 Le due circolazioni, sistemica e polmonare, sono
in parallelo e l'unico modo in cui i due circoli comunicano è tramite gli shunt
fetali attraverso il foro ovale e il dotto di Botallo e/o tramite difetti settali.
In assenza di tali shunt il difetto è incompatibile con la vita.
Le due circolazioni, sistemica e polmonare, sono
in parallelo e l'unico modo in cui i due circoli comunicano è tramite gli shunt
fetali attraverso il foro ovale e il dotto di Botallo e/o tramite difetti settali.
In assenza di tali shunt il difetto è incompatibile con la vita.
Clinica: Quando i due circoli comunicano solo tramite foro ovale e dotto di Botallo, i sintomi (cianosi e tachipena) compaiono entro le 24-48 ore dalla nascita a seguito della chiusura del dotto. Se è presente un DIV i sintomi compaiono tardivamente (nel primo mese). Può associarsi stenosi polmonare con cianosi dipendente dalla gravità della stenosi.
Diagnosi: Per la diagnosi è dirimente la dimostrazione morfologica del difetto (all'ecocardiografia è patognomonico il reperto della biforcazione polmonare dal vaso che emerge dal V. sx.). Utile il test all'iperossia che serve a indicare se la cianosi è di origine polmonare o cardiaca (si somministra ossigeno al 100% per 5 minuti: aumento della PaO2 con cianosi di origine polmonare; nessuna modificazione della PaO2 con cianosi di origine cardiaca).
In genere sono assenti segni obiettivi patologici e in caso di DIV e/o stenosi polmonare si associano i segni obiettivi di questi difetti. L'ECG può evidenziare ipertrofia ventricolare destra e l'RX torace può mostrare iperafflusso polmonare e cardiomegalia.
Trattamento: Come per la tetralogia di Fallot, anche nella trasposizione dei grossi vasi è fondamentale mantenere pervio il dotto di Botallo mediante prostaglandine. Quindi, sempre precocemente, bisogna assicurare un adeguato mixing atriale e se il forame ovale è insufficiente nel permettere un adeguato mixing, si ricorre ad una settostomia percutanea. Una volta ottenuta la stabilizzazione (in genere ad 1 settimana), si procede alla correzione chirurgica radicale e definitiva con lo switch arterioso.
Ipoplasia del ventricolo sinistro
![]()
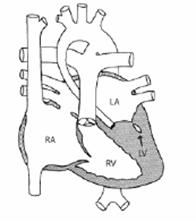 È una cardiopatia caratterizzata da ventricolo
sinistro, aorta ascendente e valvola mitrale ipoplasici e valvola aortica
atresica e rappresenta la causa di morte cardiaca più frequente in epoca
neonatale .
È una cardiopatia caratterizzata da ventricolo
sinistro, aorta ascendente e valvola mitrale ipoplasici e valvola aortica
atresica e rappresenta la causa di morte cardiaca più frequente in epoca
neonatale .
Con il forame ovale e il dotto di botallo pervi il flusso polmonare è il seguente: atrio sinistro>foro ovale (o DIA)>atrio destro>ventricolo destro>arteria polmonare>dotto di Botallo>aorta. Alla nascita la chiusura del dotto di Botallo esclude la circolazione sistemica.
Le manifestazioni cliniche sono molto gravi con cianosi, ipotensione, tachipnea e acidosi e collasso. La diagnosi richiede la dimostrazione del difetto (ecocardiografia) in quanto all'esame obiettivo non si evidenziano soffi patologici.
Anche in questo caso bisogna precocemente mantenere pervio il dotto di Botallo mediante prostaglandine. Si eseguono poi una serie di interventi palliativi gravati da elevata mortalità in attesa di trapianto cardiaco.
Atresia della tricuspide
È una cardiopatia che comprende diversi difetti cardiaci: atrofia della tricuspide, ipoplasia del ventricolo destro, DIA e DIV.
In presenza di tali difetti si ha uno shunt destro-sinistro a livello atriale (DIA) con sangue misto che fluisce nel ventricolo sinistro. Da qui il sangue misto giunge in a. polmonare (shunt sinistro-destro a livello ventricolare tramite DIV) e in aorta (per la via fisiologica).
Le manifestazioni cliniche sono cianosi (dipendente dal diametro DIV, dall'ipoplasia Vdx e dal calibro a. polmonare), che diventa molto severa in assenza di DIV (in quanto il sangue si ossigena solo attraverso dotto di Botallo pervio), e scompenso cardiaco.
Per la diagnosi l'ECG può mostrare una deviazione assiale sinistra, l'RX torace uno scarso flusso polmonare e il "cuore a zoccolo" e l'ecocardiografia evidenzia l'atresia della tricuspide e gli altri difetti.
Il trattamento, oltre al mantenimento della pervietà del dotto di botallo, consiste in interventi palliativi (shunt succlavio-polmonare, di lacerazione del DIV) e interventi correttivi (si collega l'arteria polmonare all'atrio destro e si chiude il DIV).
Scompenso cardiaco
Incapacità del cuore di adeguare la portata alle necessità metaboliche dei tessuti o di adeguarla a pressioni di riempimento e/o frequenza cardiache superiori alla norma.
Cause: In utero (rare):
Compromissione della funzione di pompa del cuore e della sua capacità a mantenere il flusso anterogrado (più che shunt od ostruzioni);
Tachicardia intrauterina sostenuta;
Anemia cronica con conseguente sovraccarico di volume;
Insufficienza miocardica secondaria a miocardite.
Età neonatale: il cuore è molto sensibile al sovraccarico di pressione ed è poco capace di gestirlo. Nel neonato a termine quindi le cause di scompenso possono essere: patologie miocardiche da asfissia, ipoglicemia, acidosi, sepsi, ipocalcemia, ostruzioni del cuore sinistro (coartazione, ipoplasia del cuore sinistro, stenosi aortica), ampi shunts (DIA, DIV, Botallo), miocarditi virali, tachi- e bradiaritmie.
Nel neonato prematuro la situazione è ancora più complessa per la scarsità di meccanismi di adattamento e di riserva funzionale per cui lo scompenso può essere precipitato da sovraccarico di liquidi, sovraccarico volumetrico per shunt sinistro-destro (Botallo pervio, DIV ampi) o cuore polmonare (da displasia broncopolmonare per esempio).
Prima infanzia (in particolare dalle 6 alle 8 settimane):
Difetto del setto interventricolare, ventricolo unico;
Tronco arterioso comune;
Pervietà del dotto arterioso;
Difetti del canale atrio-ventricolare;
Ventricolo unico;
Ritorno venoso polmonare anomalo;
Malattie metaboliche rare (malattie da accumulo di glicogeno).
Seconda infanzia:
Malattia reumatica acuta con cardite;
Cardiopatia reumatica;
Miocardite virale;
Endocardite batterica;
Sovraccarico di volume in corso di malattie non cardiache;
Tireotossicosi, emocromatosi, terapia antiblastica.
Clinica: mentre il bambino più grande presenta sintomatologia simile a quella adulta, nel lattante prevalgono i seguenti segni e sintomi:
Difficoltà ad alimentarsi, difetto di crescita;
Distress respiratorio, tachipnea (valori normali nel neonato 40-50/min);
Tachicardia (v.n. nel neonato 140-150/min);
Cardiomegalia e/o edema polmonare all'Rx;
Contrazione della diuresi;
Rantoli, rumori bronchiali (in bambini più grandi);
Epatomegalia (gli edemi periferici sono rari);
Toni di galoppo (accentuazione del 3° tono);
Colorito cutaneo pallido o cianotico;
Sudorazione eccessiva.
Terapia: la terapia dello scompenso pediatrico è nel 66% dei casi chirurgica mentre la terapia medica si avvale del riposo a letto, di Furosemide e soprattutto digitale; si associa ossigenoterapia.
Malattia reumatica
Si tratta di una complicanza acuta infiammatoria non suppurativa di una infezione da streptococco di gruppo A, caratterizzata soprattutto da artrite, corea o cardite (con possibile cardiopatia residua) presenti da sole o in combinazione; anche la pelle può essere coinvolta (noduli sottocutanei ed erythema marginatum).
Dal dopoguerra fino agli anni 80 in diminuzione per le migliorate condizioni socio-sanitarie; dal 1980 di nuovo in aumento sia negli USA che nei paesi in via di sviluppo (Asia, Africa e Sud America); in questi ultimi rappresenta una delle maggiori cause di mortalità e morbilità in età scolare.
Fattori favorenti: il sovraffollamento, la denutrizione, la carenza proteica. Più frequente nelle regioni a clima temperato umido (soprattutto in inverno e in primavera).
Età più colpita: 5-13 anni (raro < 3 anni e > 25), con massima incidenza tra 6 e 12 anni (età scolare).
Sesso: maschi e femmine in egual misura.
Eziologia e patogenesi: Streptococco beta-emolitico di gruppo A (ma oggi anche di altri gruppi, sebbene in casi rarissimi); è un germe Gram + fornito di capsula e da una membrana di tre strati:
strato esterno o proteico (proteina M : 50 sottotipi);
strato medio polisaccaridico (antigene C: 13 gruppi: A, BO);
strato interno o mucopeptidico (qui agisce la penicillina).
La patogenesi è di tipo allergico autoimmunitario: la membrana dello streptococco ha la stessa composizione antigenica della fibra miocardica e delle glicoproteine delle articolazioni e delle valvole; il sistema immunitario stimolato dall'infezione si scatena quindi contro tali strutture.
Gli immuno-complessi, depositandosi nei vari organi, contribuiscono alle lesioni. Interviene anche una disregolazione, geneticamente determinata, dell'immunità cellulare: deficit dei T suppressor con conseguente iperfunzione dei B-linfociti, produttori di auto-anticorpi.
Organi colpiti: connettivo delle capsule articolari, sierose (pericardica e pleurica), miocardio, endocardio valvolare (mitrale).
Lesioni istologiche:
fase a carattere regressivo: edema e degenerazione fibrinoide del connettivo per precipitazione di gamma-globuline nel connettivo;
fase a carattere flogistico produttivo: proliferazione delle cellule istiocitarie (cellula di Aschoff, linfociti, plasmacellule e granulociti); quando sono riunite in sede perivascolare formano il c.d. nodulo reumatico o di Aschoff (soprattutto nel tessuto miocardico);
fase sclero-riparativa: scompaiono le cellule e compaiono i fibroblasti con evoluzione verso la sclerosi (grave nelle valvole cardiache).
Clinica: Manifestazioni maggiori:
Cardite (50%):
Segni di miocardite: ingrandimento dell'aia cardiaca (Rx), tachicardia oltre 100/min (sproporzionata rispetto alla febbre), 1° tono diminuito, soffio sistolico alla punta (insuff. relativa della mitrale), aritmie cardiache: extrasistoli, blocchi A-V;
ECG: allungamento del PR e del QT; nei casi più gravi il QRS è ridotto di ampiezza e la T è piatta o negativa;
Rx: ingrandimento dell'aia cardiaca; segni di stasi nel circolo polmonare (specie in caso di pericardite);
Segni di endocardite: soffio per insufficienza mitralica (90%) e quindi sul focolaio di ascoltazione mitralica irradiato verso l'ascella;
Segni di pericardite (8%):
pericardite secca: dolore toracico e rumori di sfregamento;
pericardite essudativa: scomparsa degli sfregamenti, riduzione dei toni cardiaci;
Artrite (95%): colpisce le grandi articolazioni (come nell'adulto), ma a volte anche le piccole (mano, polso, piede); a volte vi sono interessamenti 'strani' come l'articolazione temporo-mandibolare, articolazione xifoidea, ecc. L'articolazione è molto dolente, in genere calda e arrossata, tumefatta con interessamento asimmetrico, spesso fugace e migrante;
Interessamento cutaneo (10%):
Eritema anulare o marginato: sede: tronco o arti;
Noduli cutanei o reumatici di Meynet: sottocutaneo o periarticolare (occipite, carpo, gomito, ginocchia, dorso del piede);
Eritema nodoso;
Corea minor di Sydenham (< 5%): interviene dopo 2-3 mesi dai sintomi precedenti (a volte "a ciel sereno' , cioè senza i sintomi precedenti). È dovuta a lesione del sistema extrapiramidale (nuclei della base) e del cervelletto: ciò comporta un blocco dell'azione inibitoria esercitata da questi sistemi. Ha buona prognosi con terapia anti-reazionale e sedativi (barbiturici e valproico); sintomi:
modifica dell'umore: irrequietezza, svogliatezza;
corea: movimenti involontari, rapidi e aritmici degli arti e dei m. mimici (comunque tutti muscoli possono essere interessati: es. lingua);
ipotonia muscolare con iperreflessia osteo-tendinea;
Manifestazioni minori: febbre nel 90%, alterazioni ematochimiche (in particolare indici di flogosi, TAS e streptozyme), dolori articolari vaghi, isolamento dello streptococco dal tampone, allungamento del tratto PR all'ECG.
Decorso
1a fase (infezione streptococcica): in genere localizzata al faringe o tonsille (di rado scarlattina); nel 3% dei casi si ha l'evoluzione negli altri stadi;
2a fase (di latenza o di sensibilizzazione): dura 10-15 gg, silente dal punto di vista clinico massimo astenia, mialgie) e di laboratorio;
3a fase (attacco reumatico): i sintomi della m. reumatica si possono presentare o con decorso monociclico (1-3 mesi) o con decorso policiclico (più raro) cioè con ripresa dei sintomi sospendere della terapia;
4a fase (della quiescenza o inattività): i sintomi e gli indici bio-umorali (tranne il TAS) attenuano fino a scomparire;
5a fase (delle recidive): probabilità maggiori in vicinanza dell'attacco acuto (20 % dei casi nei primi 5 anni) e in vicinanza della pubertà; più probabile il danno cardiaco.
Diagnosi: presenza di 2 manifestazioni maggiori o 1 maggiore più 2 minori (criterio di Jones).
Diagnosi differenziale: artrite settica, artriti sierose, peliosi reumatica, artrite post-enterite, artrite reumatoide, artrite di Lyme, spondiloartriti croniche.
Terapia: penicillina G i.m finché gli indici di flogosi sono positivi (in genere 2-3 settimane), poi penicillina-benzatina p.o ogni 10-14-21 gg per profilassi.
La terapia anti-reattiva invece ha lo scopo di ridurre la risposta infiammatoria e la sintomatologia: non c'è cardite FANS fino a 4-6 settimane dopo la normalizzazione degli indici di flogosi; se c'è cardite cortisonici.
Si associa riposo a letto soprattutto in caso di grave cardite, dieta povera di sodio se cortisonici eventualmente digitale e diuretici.
Esiti a distanza: si hanno quando la terapia è mal condotta. Il principale è l'insufficienza mitralica, che porta a ipertrofia del ventricolo sinistro e dilatazione dell'atrio.
Clinica: soffio olosistolico alla punta con fremito e diffusione verso l'ascella; 2° tono sulla polmonare accentuato.
Rx: ingrandimento del ventricolo e dell'atrio sinistro con compressione dell'esofago.
ECG: segni di ipertrofia ventricolare sinistra e di dilatazione atriale.
Endocarditi infettive
Infezioni microbiche dell'endocardio, caratterizzate da febbre, soffi cardiaci, petecchie, anemia, fenomeni embolici e vegetazioni endocardiche che possono esitare in insufficienza o stenosi valvolare, ascessi miocardici o aneurismi micotici.
I fattori di rischio per lo sviluppo di endocardite nel bambino sono gli stessi che per l'adulto: procedure diagnostiche invasive, cure dentarie, presenza di turbolenze di flusso intracardiache come quelle dovute alla presenza di comunicazioni tra cuore destro e sinistro, valvole mal funzionanti o aneurismi, presenza di valvole protesiche o infine chirurgia cardiaca favoriscono la batteriemia prima e l'insediamento dei batteri sul miocardio poi.
L'endocardite batterica subacuta (EBS) è di solito causata da varie specie di streptococchi (in particolare streptococchi viridans, microaerofilo e anaerobio, streptococco non-enterococco di Gruppo D ed enterococco) e, meno frequentemente, da Stafilococco aureus, S. epidermidis e da Haemophilus sp; nel bambino sono rilevanti anche Coxiella, Neisseria e Brucella. La EBS si sviluppa spesso su valvole già danneggiate e dopo batteriemie asintomatiche da infezioni del cavo orale o da infezioni genitourinarie o gastroenteriche.
L'endocardite batterica acuta (EBA) è di solito causata da S. aureus, da streptococco emolitico di Gruppo A, da pneumococco o da gonococco e da germi meno virulenti. Si può sviluppare su valvole normali.
L'endocardite su protesi valvolare (EPV) si ha nel 2-3% di pazienti entro 1 anno dall'intervento di sostituzione valvolare e nello 0,5% per anno successivamente; è più comune su protesi valvolari aortiche piuttosto che mitraliche ed è meno comune su valvole biologiche ('heterograft'). Le infezioni precoci (< 2 mesi dopo l'intervento) sono causate soprattutto da microrganismi resistenti agli antibiotici contratti al momento dell'intervento chirurgico (p. es. S. epidermidis, difteroidi, bacilli coliformi, Candida sp e Aspergillus sp). Le infezioni tardive sono causate soprattutto da microrganismi con bassa virulenza contratti durante l'intervento chirurgico o da batteriemie asintomatiche transitorie, sostenute spesso da Streptococcus sp, S. epidermidis, difteroidi e fastidiosi bacilli gram -, come Haemophilus sp, Actinobacillus actinomycetemcomitans e Cardiobacterium hominis. Lo S. epidermidis può essere un patogeno precoce o tardivo.
L'endocardite del cuore destro, che interessa la valvola tricuspide e più raramente la valvola e l'arteria polmonare, può essere provocata dall'uso di stupefacenti EV o da infezioni associate a vie venose centrali, che facilitano l'ingresso di microrganismi e possono anche danneggiare l'endocardio. I microrganismi possono provenire dalla cute (p. es., S. aureus, Candida sp o bacilli coliformi).
Nel 6% dei casi non è possibile isolare il batterio dall'emocoltura; in tali casi si deve sospettare Coxiella.
Clinica: febbre, calo di peso, debolezza, dolori articolari o muscolari, sudorazioni notturne; l'obbiettività cardiaca presenta spesso soffi di nuova insorgenza o modificazione di soffi già presenti. Spesso si associano petecchie e splenomegalia; l'endocardite può essere complicata da embolizzazione al SNC con ictus e/o ascessi cerebrali.
![]()
 Diagnosi: emocoltura, ecocardiogramma. Si possono usare i criteri di
Duke (2 criteri maggiori oppure 1 maggiore + 3 minori oppure 5 minori).
Diagnosi: emocoltura, ecocardiogramma. Si possono usare i criteri di
Duke (2 criteri maggiori oppure 1 maggiore + 3 minori oppure 5 minori).
Prognosi: nonostante la disponibilità di antibiotici la mortalità rimane del 20-25% con morbidità grave nel 50-60% dei bambini (tra cui insufficienza cardiaca dovuta alla distruzione valvolare, distruzione del sistema di conduzione, rottura del seno di Valsalva, meningite, osteomielite, ascessi).
Terapia: antibiotica per un periodo di 4-6 settimane; se possibile guidata da antibiogramma, altrimenti Penicillina G o Ceftriaxone con/senza Gentamicina; in alternativa Vancomicina.
Profilassi: ampicillina p.o 1 h prima delle procedure invasive, cure dentarie incluse.
Endocarditi non infettive
Sviluppo di un trombo sterile di piastrine e fibrina sulle valvole cardiache e sull'endocardio adiacente in risposta a trauma, locale turbolenza di flusso, immunocomplessi circolanti, vasculiti o stati di ipercoagulabilità. Le vegetazioni possono essere clinicamente non evidenziabili e rappresentano un nido per la possibile colonizzazione da parte di microrganismi circolanti; possono inoltre dar luogo a emboli o danneggiare la funzione valvolare. I cateteri che passano attraverso il cuore destro possono danneggiare le valvole tricuspide e polmonare, con il conseguente deposito di piastrine e fibrina sul sito leso.
Lesioni trombotiche più voluminose che producono importanti emboli cerebrali, renali, splenici, mesenterici, agli arti e alle arterie coronariche tendono a svilupparsi più frequentemente su una valvola cardiaca non normale, danneggiata dalla febbre reumatica o da una cardiopatia congenita; la localizzazione più frequente è la valvola mitrale, seguita dalla valvola aortica e da un interessamento combinato mitro-aortico.
Clinica: si manifesta in genere con sintomi suggestivi di embolia arteriosa. Tale patologia può anche essere sospettata quando l'ecocardiogramma mostra vegetazioni valvolari in assenza di mixoma atriale e l'emocultura risulta negativa. Può essere diagnosticata dall'esame dei frammenti degli emboli dopo l'embolectomia. La differenziazione di questa forma da un'endocardite infettiva a coltura negativa può essere difficoltosa, ma è importante, perché il trattamento con anticoagulanti orali in pazienti affetti da endocardite infettiva è associato a un'elevata incidenza di emorragie.
Miocardiopatie
Le miocardiopatie possono essere secondarie all'aumentata richeista dovuta ad esempio a malformazioni cardiache congenite; in questa sezione però sono raggruppate le affezioni che colpiscono primariamente il miocardio, per un suo difetto intrinseco o come conseguenza di alterazioni sistemiche:
le prime sono la miocardiopatia dilatativa, ipertrofica e restrittiva (trattate più nel dettaglio in seguito);
le seconde sono dovute più di frequente a: accumulo nel miocardio di metaboliti, minerali, metalli a causa di deficit enzimatici genetici (glicogenosi, tesaurismosi, iperlipidemie famigliari, emocromatosi, amiloidosi); alterazioni immunitarie (sarcoidosi, leucemie, LES, dermatomiosite, AR); infezioni batteriche o virali, anche silenti; miopatie sistemiche (distrofia muscolare, atassia di Friedrich); tumori (feocromocitoma, carcinoide); carenza di vitamine o minerali (tiamina, selenio, malnutrizione).
Miocardiopatia dilatativa
Il ventricolo appare dilatato, di solito più il sinistro. Nel 20-50% dei casi c'è familiarità, spesso per alterazioni a carico del gene della laminina, e nei casi famigliari il 5-10% si trasmette tramite il cromosoma X (spesso è colpito il gene della distrofina); possono essere coinvolti anche il genoma mitocondriale o comunque alterazioni del metabolismo degli acidi grassi.
I casi non famigliari sono spesso conseguenti a infezioni virali misconosciute, assunzione di farmaci cardiotossici o carenze alimentari.
Clinica: tutte le età possono essere colpite. L'esordio è insidioso con anoressia, irritabilità, dispnea da congestione polmonare nei più piccoli, e prevalenza di sintomi addominali aspecifici nei bambini più grandi. Con il procedere della malattia si instaurano i segni e i sintomi di insufficienza cardiaca di tipo sistolico (tachicardia, pallore, polsi periferici lievi).
Diagnosi: l'ECG mostra un aumento dell'atrio, del ventricolo e anomalie di ripolarizzazione. All'RX torace l'OCV è aumentata con grado variabile di congestione polmonare.
Prognosi e terapia: la prognosi è grave, e la terapia è quella dello scompenso, ovvero volta a sostenere la funzione miocardica residua. Si valuta il trapianto cardiaco.
Miocardiopatia ipertrofica
Più spesso della precedente questa miocardiopatia è dovuta a cardiopatia congenita, con aumento delle richieste tale da provocare una massiccia ipertrofia del miocardio.
I casi primitivi sono dovuti a mutazione delle proteine del sarcomero, che in gradi diversi si manifesta in un individuo su 500; in questi casi l'ipertrofia prevale a carico del setto, causando anche un'ostruzione all'efflusso.
Clinica: nel 50% è asintomatica; nei casi sintomatici vi sono debolezza, dispnea, palpitazioni, angina e sincopi. Può essere presente un soffio che si accentua durante la manovra di Valsalva o nell'assumere la posizione eretta. La disfunzione è primariamente diastolica.
Diagnosi: l'ECG mostra ipertrofia ventricolare con ST sottoslivellato e alterazioni della T; l'Rx mostra prominenza ventricolare. Il Doppler rivela le alterazioni di flusso date dall'ostruzione settale.
Prognosi e terapia: la prognosi è variabile; il trattamento prevede astensione dagli sport vigorosi a causa dell'aumentato rischio di morte improvvisa. I beta bloccanti possono essere utili anche se non modificano la prognosi; nei soggetti a rischio di aritmia si valuta il defibrillatore.
Miocardiopatia restrittiva
Il ventricolo appare rigido, poco compliante e si riempie a fatica provocando ristagno a monte. Si associa a patologie del connettivo, sd. ipereosinofila, tumori maligni o irradiazione dell'area.
Clinica: si manifesta con i segni e sintomi dello scompenso congestizio.
Diagnosi: l'ECG mostra onde P alte, ST sottoslivellato, T invertita e QRS nella norma. L'ecocardio mostra atri ingranditi e ventricoli nella norma il cui riempimento è anomalo.
Prognosi e terapia: la prognosi è pessima, il trattamento è quello dello scompenso congestizio ma non è molto efficace. Si invia il pz al trapianto.
Fonti: www.msd-italia.it; Pediatria di Zappulla, Pediatria di Nelson e appunti delle lezioni.
 |
|
| Appunti Bellezza |  |
| Tesine Nutrizione |  |
| Lezioni Bambini |  |