 |
|
| Appunti tecniche |
|
 |
|
| Appunti tecniche |
|
| Visite: 4265 | Gradito: |
Leggi anche appunti:Tesina MECCANICA - Ruote dentateTesina classe Prove con il carburatore elettronico comandato in retroazioneProve con il carburatore elettronico comandato in retroazione 1 BiomeccanicaBIOMECCANICA Il moto è il risultato più importante |
 |
 |
I numeri quantici e l'atomo di Idrogeno
Come la seconda legge di Newton, l'equazione di Schrödinger è un'equazione differenziale del secondo ordine dotata di un'ampia applicabilità. Infatti, vale per tutti i sistemi atomici purché la velocità degli elettroni non sia confrontabile con la velocità della luce. La conoscenza delle funzioni d'onda permette di fare previsioni riguardo alla posizione, alla quantità di moto e all'energia della microparticella in questione. Lo stato di ogni particella è descrivibile mediante quattro soli numeri che sono soluzioni della funzione d'onda y(x,y,z); questi numeri sono denominati numeri quantici.
I. NUMERO QUANTICO PRINCIPALE (n):
può
assumere valori interi positivi ![]() e determina l'energia
dell'orbita stazionaria secondo l'equazione di Bohr:
e determina l'energia
dell'orbita stazionaria secondo l'equazione di Bohr:
![]()
nello specifico per l'atomo di idrogeno vale la relazione:
![]()
II. NUMERO QUANTICO ORBITALE (l):
Per un dato numero quantico principale n, il numero quantico orbitale l,
assume i valori possibili: ![]() e determina il momento
della quantità di moto dell'elettrone (o della microparticella in generale). Un
elettrone con un determinato valore di l
avrà un momento della quantità di moto uguale a:
e determina il momento
della quantità di moto dell'elettrone (o della microparticella in generale). Un
elettrone con un determinato valore di l
avrà un momento della quantità di moto uguale a:
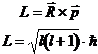
Anche il momento angolare dell'elettrone è quantizzato come la sua energia. Esso può assumere soltanto i valori dati dall'equazione precedente
III. NUMERO QUANTICO MAGNETICO (![]() ):
):
Per un dato numero quantico orbitale l, il numero quantico
magnetico m specifica la
componente del momento angolare secondo una certa direzione fissa, in altre
parole fornisce informazioni circa l'orientazione del momento angolare lungo
una direzione, denominata z. Per
ciascun l esistono ![]() valori permessi di m:
valori permessi di m: ![]() .
.
La componente del momento angolare lungo l'ipotetico asse z è data da:
![]()
E' usato il prefisso magnetico poichè questo numero quantico serve a descrivere la scissione delle righe spettrali in componenti discrete nel caso di atomi collocati in un intenso campo magnetico. Questa scissione è detta effetto Zeeman dal nome dello scienziato che osservò tale fenomeno nel 1896. Il vettore momento angolare orbitale non può avere un orientamento arbitrario nello spazio nel campo magnetico bensì quantizzato.
IV. SPIN (s) E NUMERO QUANTICO DI
SPIN (![]() ):
):
Ogni elettrone possiede un momento angolare intrinseco S in funzione di un numero quantico s. Quest'ultimo numero, detto spin, secondo le ipotesi di S. Goudsmit e G. Uhlenbeck, fig.(15-b), può assumere soltanto valore uguale a 1/2. Inoltre, essendo analogo al numero quantico orbitale l, il modulo del vettore S risulterà, parimenti a quello del vettore L:
![]()
di
conseguenza le possibili orientazioni di S
su un qualsiasi asse arbitrario z
sono date dalla formula: ![]() con
con ![]() . Il termine spin
in inglese significa trottola e si
giustifica con l'idea intuitiva che il momento
angolare intrinseco dell'elettrone sia dovuto alla rotazione della sua
massa e della sua carica attorno ad un asse. In realtà quest'interpretazione è
in completo disaccordo con i dati sperimentali per cui l'elettrone è un oggetto
puntiforme e non un corpo esteso. Lo spin
dell'elettrone non è quindi una grandezza legata al suo stato di moto, come la
velocità o l'energia cinetica, ma piuttosto è una caratteristica intrinseca
della sua natura, come la sua massa e la sua carica. Il numero di spin assume numeri anche differenti da
1/2 per particelle diverse dall'elettrone. In generale il mondo delle
particelle viene classificato in base allo spin
in due grandi famiglie: i bosoni
aventi spin intero e i fermioni avente spin semidispari.
. Il termine spin
in inglese significa trottola e si
giustifica con l'idea intuitiva che il momento
angolare intrinseco dell'elettrone sia dovuto alla rotazione della sua
massa e della sua carica attorno ad un asse. In realtà quest'interpretazione è
in completo disaccordo con i dati sperimentali per cui l'elettrone è un oggetto
puntiforme e non un corpo esteso. Lo spin
dell'elettrone non è quindi una grandezza legata al suo stato di moto, come la
velocità o l'energia cinetica, ma piuttosto è una caratteristica intrinseca
della sua natura, come la sua massa e la sua carica. Il numero di spin assume numeri anche differenti da
1/2 per particelle diverse dall'elettrone. In generale il mondo delle
particelle viene classificato in base allo spin
in due grandi famiglie: i bosoni
aventi spin intero e i fermioni avente spin semidispari.
Esistono dunque
quattro numeri quantici in grado di descrivere completamente (o quasi) gli
stati di tutte le particelle costituenti il nostro mondo fisico, anche se in realtà,
col progredire della teoria e delle nuove scoperte permesse dall'utilizzo di
acceleratori e collisori con energie sempre più elevate, è stato necessario
aggiungerne un quinto: il colore.
Questo nuovo numero quantico sarebbe in grado di descrivere gli stati e le
trasformazioni delle particelle elementari tra cui i quark, ultimi costituenti
del nucleo e oggetto della particella mediatrice della forza nucleare forte: il
gluone.
 |
| Appunti su: appuntimania, |
|
| Appunti Aeronautica |  |
| Tesine costruzione |  |
| Lezioni Silvicoltura |  |