 |
|
| Appunti scientifiche |
|
 |
|
| Appunti scientifiche |
|
| Visite: 8654 | Gradito: |
Leggi anche appunti:Energia di prima ionizzazioneEnergia di prima ionizzazione Viene definita come l'energia, espressa in I miscugliI miscugli Combustori a bassa emissione di inquinantiCOMBUSTORI A BASSA EMISSIONE DI INQUINANTI 1.1. Introduzione Nel |
 |
 |
A differenza dei conformeri, gli isomeri configurazionali sono degli stereoisomeri che, pur mantenendo la medesima connettività (i collegamenti tra i singoli atomi rimangono i medesimi), possono essere trasformati l'uno nell'altro solo rompendo legami chimici.
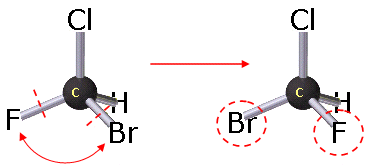
Isomeri
configurazionali - la connettività si conserva (il Fluoro, il Bromo, il Cloro e
l'Idrogeno sono legati al Carbonio in entrambi gli isomeri), ma per
trasformare un isomero nell'altro è necessario rompere i legami C-F e C-Br
e scambiare di posizione gli atomi di Fluoro e Bromo
L'isomeria configurazionale è una forma di isomeria spaziale (stereoisomeria) che si divide in enantiomeria e diastereoisomeria.
Sono enantiomeri gli isomeri configurazionali chirali. Si definisce chirale (dal greco = cheir = mano) una molecola che non è sovrapponibile alla sua immagine speculare.
Sono diastereoisomeri gli isomeri configurazionali achirali, che non sono uno l'immagine speculare dell'altro.
Alcuni autori definiscono diastereoisomeri tutti gli stereoisomeri che non sono enantiomeri, comprendendo quindi tra i diastereoisomeri anche i conformeri. Lo schema di classificazione in questo caso diventerebbe il seguente
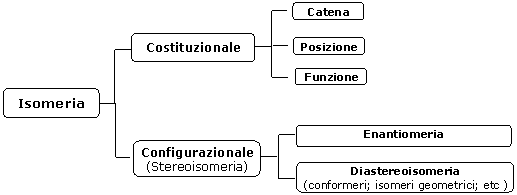
Noi tuttavia ci atterremo qui allo schema di classificazione presentato all'inizio della trattazione.

ENANTIOMERIA o ISOMERIA OTTICA
L'enantiomeria o isomeria ottica è una forma di isomeria configurazionale che deriva dalla presenza di molecole chirali, che non sono sovrapponibili alla loro immagine speculare.
Si noti che se l'immagine speculare di una molecola fosse ad essa sovrapponibile, non si tratterebbe di un nuovo stereoisomero, ma della medesima molecola.
Le molecole chirali di gran lunga più diffuse sono dovute alla presenza di un atomo di carbonio tetraedrico asimmetrico, un carbonio ibridato sp3 tetrasostituito (legato a 4 gruppi chimici uno diverso dall'altro e spesso indicato con un asterisco *).
Ne sono un esempio i due enantiomeri dell'amminoacido alanina.
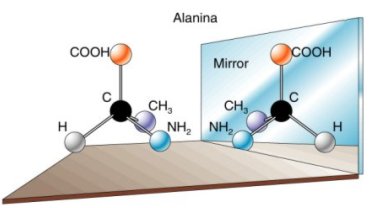
Per la sua capacità di generare stereoisomeri, l'atomo di Carbonio tetraedrico asimmetrico viene definito stereogenico.
La stereogenicità è la proprietà che possiede una struttura atomica, per questo detta struttura stereogenica, di produrre un nuovo stereoisomero come conseguenza dello scambio tra due atomi (o gruppi chimici) ad essa legati (inversione).
Le strutture stereogeniche (o elementi stereogenici) possono rendere chirali le molecole in cui si trovano, ma ciò non avviene sempre necessariamente.
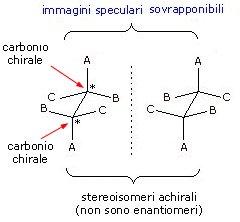
La presenza di una struttura stereogenica non rende dunque automaticamente chirale una molecola.
Sono strutture stereogeniche i centri stereogenici (come l'atomo di Carbonio asimmetrico), gli assi stereogenici ed i piani stereogenici, spesso impropriamente detti centri chirali, assi chirali e piani chirali.
L'aggettivo "chirale" andrebbe infatti usato per indicare l'intera molecola (ovviamente se essa è chirale) e non una parte di essa. La chiralità è infatti una proprietà dell'intera molecola e non di un atomo o di un gruppo di atomi al suo interno.
Se una molecola risulta chirale come conseguenza della presenza di una di queste strutture stereogeniche, allora si parla di chiralità centrale, chiralità assiale e chiralità planare, Esistono infine molecole chirali come conseguenza di una struttura elicoidale. La chiralità elicoidale è anche detta elicità.
La chiralità assiale si genera quando due coppie di sostituenti, ciascuno diverso dall'altro all'interno di una medesima coppia, si trovano legate alle due estremità di una struttura molecolare rigida allungata (asse stereogenico o, impropriamente, asse chirale), in modo da presentarsi sfalsati, se osservati lungo l'asse stereogenico.
E' possibile immaginare un asse stereogenico come il risultato di uno stiramento di un centro stereogenico tetraedrico
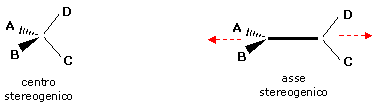
Mentre un centro stereogenico tetraedrico per generare un composto chirale deve possedere 4 sostituenti diversi (a b c d), un asse stereogenico per generare un composto chirale è sufficiente che presenti i due sostituenti di ogni coppia diversi tra loro. Risultano pertanto chirali anche i composti del tipo
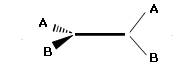
Un esempio di asse stereogenico si ha con gli alleni. Gli alleni presentano due doppi legami adiacenti separati da un carbonio ibridato sp. L'asse stereogenico è costituito dal gruppo C=C=C. Ciascun doppio legame giace su di un piano perpendicolare rispetto all'altro formando una struttura lineare rigida che costringe i sostituenti alle due estremità dell'asse stereogenico ad assumere una conformazione sfalsata stabile. Gli alleni sono chirali solo se i due sostituenti che formano ciascuna coppia sono tra loro diversi. Se nella molecola sono presenti più assi stereogenici (più doppi legami cumulati) l'allene può essere chirale solo se possiede un numero dispari di doppi legami cumulati.
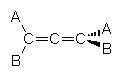

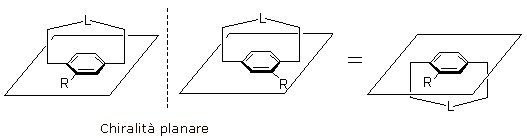
La chiralità planare si genera quando un gruppo di atomi disposti su di un piano (piano stereogenico o, impropriamente, piano chirale) sono connessi ad una struttura rigida (spesso a ponte) che si estende sopra o sotto il piano.
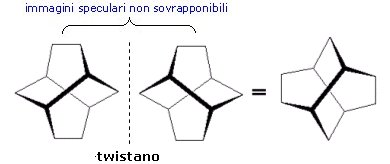
La chiralità elicoidale o elicità si genera quando la molecola presenta una configurazione avvitata (elicoiale). Le molecole di questo tipo possono presentarsi in due forme enantiomeriche, distinguibili in relazione al senso di avvitamento destrorso o sinistrorso.
Ne è un esempio il twistano , un triciclodecano formato da anelli fusi di cicloesano in conformazione a treccia (twist)
Attività ottica degli enantiomeri
Gli enantiomeri hanno proprietà fisiche identiche (p. ebollizione, p. fusione, solubilità etc), ad eccezione dell'attività ottica e proprietà chimiche identiche, con l'esclusione della interazione con reattivi chirali (otticamente attivi).
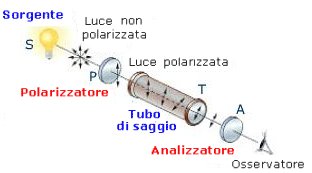
Si definisce attività ottica la capacità di una molecola di ruotare il piano della luce polarizzata. In particolare quando una luce polarizzata, che vibra lungo un solo piano, attraversa una soluzione contenente una molecola chirale il suo piano di vibrazione viene ruotato di un certo angolo [] che dipende dalla concentrazione, dalla lunghezza d'onda della luce monocromatica, dalla temperatura, dal solvente usato e dalla lunghezza del percorso ottico.
Per standardizzare i valori delle
attività ottiche si è adottata come unità di misura la rotazione specifica (o potere rotatorio specifico) ![]() misurata ad una certa temperatura (in genere t = 25° C)
e ad una certa lunghezza d'onda (in genere = 589 nm riga D dello spettro di emissione del sodio)
misurata ad una certa temperatura (in genere t = 25° C)
e ad una certa lunghezza d'onda (in genere = 589 nm riga D dello spettro di emissione del sodio) ![]() :
:

La misura dell'attività ottica è molto comune e serve a distinguere gli enantiomeri fra di loro. Due enantiomeri, a parità di condizioni, ruotano infatti il piano della luce polarizzata del medesimo angolo, ma in senso opposto. L'enantiomero che produce una rotazione in senso orario (destrogiro) viene indicato con il segno (+), mentre quello che produce una rotazione in senso antiorario (levogiro) con il segno (-). I due enantiomeri vengono anche definiti antipodi ottici. Un sistema contenente un ugual numero di molecole dei due enantiomeri non presenta attività ottica, viene contraddistinto dal simbolo (±) posto davanti al nome del composto e si definisce miscela racemica o racemo.
Una miscela in cui uno dei due enantiomeri è presente in maggiore quantità mostrerà una rotazione ottica proporzionale alla percentuale della specie in eccesso.
Una miscela racemica non può essere separata dai suoi componenti mediante i comuni metodi fisici (cristallizzazione, distillazione etc.). Per la separazione si deve prevedere l'uso di specie chirali che interagiscono diversamente con le due molecole di differente chiralità. Nei sistemi biologici, ad esempio, questo ruolo è svolto dagli enzimi che sono in grado di metabolizzare una forma enantiomerica lasciando l'altra inalterata.
Configurazione di una molecola chirale: stereodescrittori R/S
I due enantiomeri di una molecola chirale differiscono solamente per la disposizione spaziale dei loro sostituenti intorno alla struttura stereogenica. Presentano cioè una diversa configurazione.
Per definire univocamente il nome e la configurazione assoluta degli enantiomeri si ricorre alle regole di Cahn-Ingold-Prelog (regole CIP) che permettono di assegnare a ciascuno sostituente dello stereocentro un ordine di priorità.
Regole di Cahn-Ingold-Prelog
1. La priorità viene attribuita sulla base del numero atomico. Più elevato è il numero atomico più alta è la priorità del sostituente. Per esempio: 17Cl > 8O > 7N > 6C > 1H
2. A parità di numero atomico (isotopi), la priorità spetta all'isotopo con massa atomica maggiore. Così il trizio, l'isotopo dell'idrogeno con massa di 3 uma, ha priorità più alta del deuterio che ha massa atomica di 2 uma. L'idrogeno, che ha numero atomico 1 e massa atomica di 1 uma, ha la più bassa priorità non soltanto rispetto ai suoi isotopi, ma anche rispetto a tutti gli altri elementi della tavola periodica.
3. Se l'applicazione delle due regole precedenti non permette di assegnare la priorità, significa che i due atomi confrontati sono uguali ed è allora necessario esaminare e confrontare ordinatamente gli altri atomi a cui sono necessariamente legati (se non fossero legati ad altri atomi i due sostituenti sarebbero uguali e non vi sarebbe stereoisomeria). Si procede pertanto, sempre applicando le regole precedenti, al confronto degli atomi successivi in entrambe le catene fino al punto in cui si individua una differenza di priorità.
per esempio.
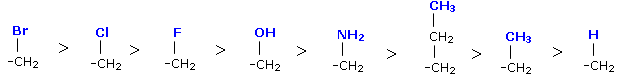
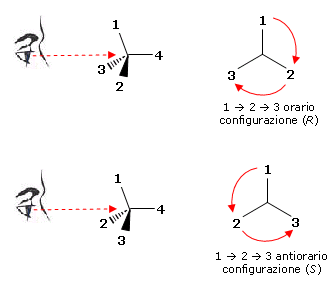
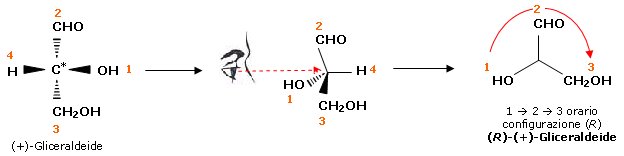
Una volta che la priorità CIP sia stata assegnata ai gruppi legati allo stereocentro, si orienta la molecola in modo tale che il sostituente a più bassa priorità (4) sia diretto lontano dall'osservatore, mentre i gruppi a priorità più elevata (1,2,3) siano rivolti verso l'osservatore.
A questo punto, se per andare ordinatamente dal gruppo a priorità maggiore a quello a priorità minore (1 3) si procede in senso orario, si assegna allo stereocentro la configurazione R (dal latino rectus, quindi "destrorsa").
Se, invece, si procede in senso antiorario, si assegna allo stereocentro la configurazione S (dal latino sinister, quindi "sinistrorsa"). Si scrive R ed S in corsivo (italico) e non R ed S
Assegniamo ad esempio la configurazione assoluta alla (+)-Gliceraldeide
DIASTEREOISOMERIA
Tutti gli isomeri configurazionali che non sono enantiomeri sono, per definizione, diastereoisomeri. Si definiscono pertanto diastereoisomeri, gli isomeri configurazionali che non sono l'immagine speculare l'uno dell'altro (ed ovviamente non sono neppure sovrapponibili, altrimenti sarebbero il medesimo composto).
La forma più nota e diffusa di diastereoisomeria è l'isomeria geometrica o isomeria cis-trans.
L'isomeria geometrica è una forma di isomeria configurazionale che deriva dalla presenza nella molecola di un elemento di rigidità (doppio legame Carbonio-Carbonio, anello ciclico) che impedisce alla molecola di ruotare liberamente e completamente attorno ad un legame Carbonio-Carbonio. Gli isomeri geometrici hanno proprietà fisiche diverse (punto di fusione, punto di ebollizione, densità, indice di rifrazione diversi) e sono quindi fisicamente separabili.
Il doppio legame carbonio-carbonio, oltre a conferire allo scheletro molecolare una disposizione planare, impedisce ad esempio alla molecola di ruotare attorno all'asse del legame. Si dice che non vi è libera rotazione attorno ad un doppio legame. Da ciò deriva l'esistenza di forme isomere che differiscono, per la posizione spaziale statica (configurazione) di due sostituenti, a seconda che questi ultimi si dispongano dalla stessa parte (isomero cis) o su lati opposti (isomero trans) rispetto al doppio legame. Prendiamo ad esempio in considerazione i seguenti 2 isomeri geometrici del 2-butene.
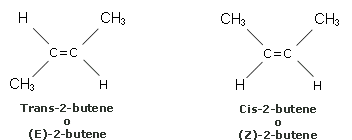
Ciascun composto ha formula grezza C4H8, ma la disposizione dei gruppi rispetto ai due atomi di carbonio legati con doppio legame è diversa. In particolare nell'isomero cis i due gruppi metilici si trovano dallo stesso lato rispetto al doppio legame, mentre nell'isomero trans si trovano su lati opposti. La stessa situazione si ripete ovviamente anche per gli atomi di idrogeno.
Si noti che il butene presenta altri due isomeri (non geometrici): un isomero di posizione (1-butene) ed uno di catena (isobutene)
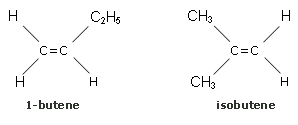
Entrambi questi isomeri non sono isomeri geometrici. Infatti, l'isomeria geometrica non può esistere se uno dei due atomi impegnati nel doppio legame è legato a due gruppi uguali:
Gli isomeri geometrici presentano due diverse configurazioni e non è possibile passare dall'una all'altra senza rompere il doppio legame.
Esistono alcuni isomeri geometrici che non possono essere classificati usando il metodo cis/trans, ad esempio quelli che presentano i due atomi di carbonio impegnati nel doppio legame legati a 4 sostituenti diversi. Prendiamo ad esempio in considerazione i due isomeri del 1-bromo-1-cloro-1-propene.
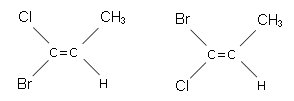
Quale dei due alogeni, il bromo o il cloro, deve essere considerato in posizione trans rispetto al metile e quale in posizione cis?
Per superare questa difficoltà la IUPAC ha introdotto un metodo differente di nomenclatura per gli isomeri geometrici degli alcheni, che utilizza gli stereodescrittori E/Z. Il metodo prevede di assegnare a ciascuno sostituente un ordine di priorità utilizzando le regole di Cahn-Ingold-Prelog.
Secondo il metodo E/Z:
1) Le due estremità del doppio legame vengono considerate separatamente.
2) utilizzando le regole di Cahn-Ingold-Prelog si individua il gruppo a maggior priorità tra i due gruppi di destra ed il gruppo a maggior priorità tra i due gruppi di sinistra (ovviamente affinché ci possa essere isomeria geometrica i due gruppi ad ogni estremità devono essere tra loro differenti
3) Il prefisso (E) (entgegen = opposti) viene assegnato allo stereoisomero in cui i due gruppi a maggior priorità si trovano ai lati opposti rispetto al doppio legame
4) Il prefizzo (Z) (zusammen = insieme) viene assegnato allo stereoisomero in cui i due gruppi a priorità più elevata si trovano dallo stesso lato del doppio legame.
Il fenomeno della isomeria geometrica si ritrova in tutte le classi di composti che contengono un doppio legame. Esistono tuttavia esempi di isomeria geometrica anche in composti privi di doppi legami. È il caso ad esempio dei cicloalcani disostituiti, in cui i due gruppi sostituenti possono trovarsi dalla stessa parte (cis) o da parti opposte (trans) rispetto al piano dell'anello.
Ad esempio il cicloesano, nella sua conformazione più stabile (a sedia), può legare 2 sostituenti entrambi dallo stesso lato del piano dell'anello, formando un isomero cis, oppure ai lati opposti, formando un isomero trans
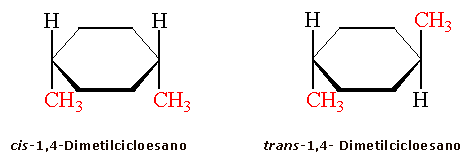
Formano diastereoisomeri anche molecole con più di un atomo di carbonio asimmetrico.
Consideriamo ad esempio la seguente molecola che presenta due atomi di carbonio asimmetrici (indicati con gli asterischi).
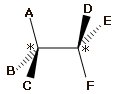
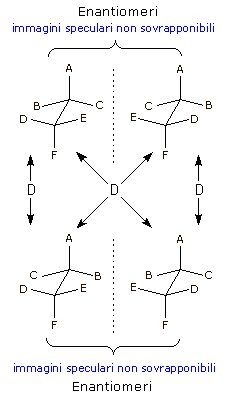
Nello schema successivo sono rappresentati i suoi 4 isomeri configurazionali. Tra essi vi sono due coppie di enantiomeri (uno l'immagine speculare non sovrapponibile dell'altro) e 4 coppie di diastereoisomeri.
 |
|
| Appunti Biologia |  |
| Tesine Ingegneria tecnico |  |
| Lezioni Geografia |  |