 |
|
| Appunti scientifiche |
|
 |
|
| Appunti scientifiche |
|
| Visite: 3487 | Gradito: |
Leggi anche appunti:Modulo di Metodi Fisici in Chimica OrganicaCorso di Metodi Fisici in Chimica Organica e Chimica Analitica Per Biotecnologie Acidi nucleici: DNA ed RNAAcidi nucleici: DNA ed RNA Gli acidi nucleici sono l'acido desossiribonucleico Passaggi di statoPASSAGGI DI STATO œ Scopo dell'esperimento Attraverso quest'esperienza intendiamo |
 |
 |
Sono composti caratterizzati dal gruppo funzionale - OH.. Ci sono alcoli saturi, insaturi, ciclici, aromatici, primari, secondari, terziari (secondo che l'OH sia legato ad un carbonio primario, secondario, terziario); monovalenti, bivalenti, polivalenti (se contengono uno, due o più ossidrili). I fenoli sono gli alcoli in cui l'OH è legato al carbonio di un anello aromatico.
La desinenza ufficiale della funzione - OH è - olo. La numerazione delle catene è fatta in modo da attribuire all'OH (o agli -OH ) i numeri più piccoli possibili.
Vi sono anche nomi d'uso comune conservati (indicati in parentesi). In casi complessi il gruppo - OH viene chiamato idrossi.
H H H H OH H
| | | | | |
H− C−OH H−C−C− OH H−C− C − C−H
| | | | | |
H H H H H H
(alcol metilico) (alcol etilico) (alcol isopropilico)
alcol primario monovalente saturo alcol primario monovalente saturo alcol secondario monovalente saturo
[137] [138]
OH OH OH OH
| | | |
 H− C − C − C −H
H− C − C − C −H
H H H CH2=CH - CH2OH
1,2,3 PROPANTRIOLO CICLOESANOLO 2-PROPEN-1-OLO
(glicerina) (alcol allilico)
alcol primario 2 volte, secondario alcol secondario monovalente alcol primario monovalente
1 volta, trivalente, saturo ciclico insaturo.
[139] [140] [141]
FENOLO C6H5OH [142]: alcol secondario, monovalente, aromatico.
DI-DROSSIBENZENI (o-, m-, p-) [143]: alcoli secondari, bivalenti, aromatici.
OH

 |
|
 OH
OH
![]()
![]()
![]() [143]
[143]
OH
![]() La presenza dell'ossidrile
conferisce agli alcoli la possibilità di formare legami idrogeno
intermolecolari (R - O H - O -
R ) che ne innalzano il punto di
ebollizione rispetto agli idrocarburi a pari atomi
La presenza dell'ossidrile
conferisce agli alcoli la possibilità di formare legami idrogeno
intermolecolari (R - O H - O -
R ) che ne innalzano il punto di
ebollizione rispetto agli idrocarburi a pari atomi
| H
H │
![]() di carbonio, e legami idrogeno con l'acqua (R -
O H - O - H ) che ne aumenta
la solubilità in tale solvente.
di carbonio, e legami idrogeno con l'acqua (R -
O H - O - H ) che ne aumenta
la solubilità in tale solvente.
Si sono già incontrati alcuni metodi di preparazione degli alcoli: idratazione degli alcheni[ ], ossidrilazione degli alcheni con permanganato[ ], idrolisi degli alogenuri (SN, [ ]). Un altro metodo generale per ottenere gli alcoli, in particolare quello etilico, consiste nella fermentazione di zuccheri da parte di microrganismi (saccaromiceti). La preparazione dei fenoli ricorre alla fusione alcalina degli acidi solfonici:
SO3H OH
![]()

![]()

![]()
![]() KOH
KOH
![]() + K2 SO3
+ K2 SO3
![]() 300°C
300°C
ACIDO BENZENSOLFONICO FENOLO SOLFITO DI
POTASSIO
Le reazioni degli alcoli si distinguono a seconda del legame che viene rotto :
![]()
![]()
![]()
![]() R OH oppure RO H
R OH oppure RO H
Tra le prime si ricordano la DISIDRATAZIONE che porta alla formazione di alcheni [ ]e la trasformazione in alogenuri alchilici [125].
Tra le seconde:
Carattere acido base: gli alcoli grazie alla loro stretta somiglianza con l'acqua (R - O - H, H - O - H ), hanno comportamento anfotero, cioè vengono protonati [143] dagli acidi forti (comportamento basico) e salificati dalle basi forti (comportamento acido).
![]() R - O - H + H+ R - O + - H
R - O - H + H+ R - O + - H
|
H
![]() R - O - H + Na R - O−
Na + + ½ H2
R - O - H + Na R - O−
Na + + ½ H2
I loro sali sono chiamati alcolati [144] e vengono facilmente idrolizzati dall'acqua, trattandosi di sali di acido debole e base forte (come acido un alcol ha una Ka 10-16). I sali dei fenoli sono invece stabili in soluzione acquosa, avendo i fenoli una Ka
Ossidoriduzione: gli alcoli sono da considerarsi come gruppi relativamente ridotti, per cui si prestano a reazioni di ossidazione (deidrogenazioni) che trasformano gli alcoli primari in aldeidi [145] e quelli secondari in chetoni[146]. Gli alcoli terziari in generale danno prodotti di ossidazione nei quali si è persa l'identità dello scheletro dell'alcol di partenza.
H H

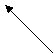 R - C - O R - C = O
R - C - O R - C = O
| | ALDEIDE
H + K2Cr2C7 H

- H2
H H
| |
R - C - O R - C = O CHETONE
| |
R' R'
Formazione di eteri: per disidratazione di alcoli si ottengono i corrispondenti eteri [147].
- H2O
![]() R - O -
H + H - O - R R - O - R
R - O -
H + H - O - R R - O - R
Si noti che già si è detto che la disidratazione di alcoli porta ad alcheni [ ]. Le due cose non sono contrastanti in quanto la disidratazione di un alcol può essere sia intramolecolare [ ] che intermolecolare [147], a seconda delle condizioni sperimentali in cui la reazione viene condotta e, per bene che vadano le cose, si ottengono sempre o alcheni contaminati da eteri o eteri contaminati da alcheni.
Formazione di esteri: per disidratazione intermolecolare tra un acido e un alcol si formano esteri [148].
O O
|| ||
![]() R - O - H + H
- O - C - R R - O - C
- R
R - O - H + H
- O - C - R R - O - C
- R
H2O
![]()
![]() Alcool metilico CH3OH
[136]: liquido infiammabile, punto di ebollizione 65°C, molto velenoso.
Si ottiene industrialmente per sintesi da ossido di carbonio e idrogeno ( CO +2H2
CH3OH).
Alcool metilico CH3OH
[136]: liquido infiammabile, punto di ebollizione 65°C, molto velenoso.
Si ottiene industrialmente per sintesi da ossido di carbonio e idrogeno ( CO +2H2
CH3OH).
Alcool etilico CH3CH2OH [137]: liquido infiammabile, punto di ebollizione 78,5°C. Quello destinato ad uso alimentare è al 95%; è possibile ottenere alcol al 100%, chiamato assoluto. Per uso non alimentare viene denaturato per aggiunta di metanolo, toluene, sostanze maleodoranti e coloranti, godendo in tal modo di particolari sgravi fiscali.
Glicole etilenico CH2OHCH2OH oppure CH2−- CH2 [ ]
| |
OH OH
Liquido solubilissimo in acqua, punto di ebollizione 197°C, usato come anticongelante e, sotto forma di etere nitrico, come esplosivo.
Fenolo C6H5OH [142]: solido, punto di fusione 43°C, poco solubile in acqua, velenoso e caustico. È usato come disinfettante e per produrre materie plastiche, concianti, coloranti, esplosivi e prodotti farmaceutici.
Glicerina CH2OH−CHOH−CH2OH oppure CH2 - CH - CH2 [ ] :
| | |
OH OH OH
Liquido oleoso solubilissimo in acqua, punto di ebollizione 290°C, di sapore dolciastro, di cui sono noti oltre 1500 impieghi (solvente, plastificante, emolliente, in profumeria e cosmesi, nella stampa, come antigelo, per produrre la nitroglicerina).
Cresoli [149]:

OH

![]()
CH3
sono i tre metilfenoli isomeri (orto, meta, para). Si trovano nel catrame e sono velenosi. Sono disinfettanti energici e costituiscono materia prima per fare coloranti , profumi, esplosivi.
 |
|
| Appunti Geografia |  |
| Tesine Biologia |  |
| Lezioni Ingegneria tecnico |  |