 |
|
| Appunti scientifiche |
|
 |
|
| Appunti scientifiche |
|
| Visite: 3308 | Gradito: |
Leggi anche appunti:L'impressionismo - paul gauguin, paul cezanneL'Impressionismo Nella seconda metà dell'Ottocento era ancora molto Combustori a bassa emissione di inquinantiCOMBUSTORI A BASSA EMISSIONE DI INQUINANTI 1.1. Introduzione Nel Le proprietà colligativeLe proprietà colligative Parlando di soluzioni binarie solido-liquido, possiamo |
 |
 |
Corso di Metodi Fisici in Chimica Organica e Chimica Analitica Per Biotecnologie Farmaceutiche
Modulo di Metodi Fisici in Chimica Organica
Lezione 6
Come già accennato in diversi punti nelle precedenti lezioni il fenomeno della risonanza magnetica nucleare può essere applicato non solo al nucleo dell'idrogeno ma anche ad altri elementi i cui nuclei siano magneticamente attivi. Un nucleo si definisce magneticamente attivo quando posto in un campo magnetico è in grado di assumere due o più orientamenti ad ognuno dei quali è associato un diverso livello energetico. Le transizioni tra livelli generate dall'interazione con una opportuna radiazione elettromagnetica (dell'ordine delle radiofrequenze) opportunamente rilevate danno luogo ad uno spettro di risonanza magnetica che abbiamo fino ad ora analizzato nel dettaglio nel caso dell'idrogeno.
In particolare l'idrogeno assume in un campo magnetico due orientamenti, alfa e beta, poiché possiede spin = 1/2. Il numero di orientamenti è infatti dato da
2I + 1 dove I è il numero quantico di spin
Se osserviamo la tabella notiamo anche che l'idrogeno (come isotopo fondamentale 1H) ha una abbondanza naturale praticamente del 100%. Questo significa che tutti i nuclei di idrogeno presenti in una molecola 'contribuiscono' alla creazione del segnale NMR e di conseguenza la sensibilità relativa dell'idrogeno è pari a 1. Anche la sensibilità assoluta, definita come il prodotto tra sensibilità relativa ed abbondanza naturale, è nel caso dell'idrogeno pari a 1. Nella tabella viene poi riportata la frequenza di risonanza del nucleo osservato in un campo magnetico di 4.7 tesla. La frequenza di risonanza data da
= B0/2
nel caso dell'idrogeno con = 26.7 è pari a 200 MHz. Le ultime due colonna della tabella riportano rispettivamente il composto di riferimento su cui si costruisce la scala in ppm (nel caso dell'idrogeno il tetrametilsilano, TMS) e l'intervallo in ppm in cui possono essere osservati, cioè risuonano, praticamente tutti i nuclei (Fig.1).
|
isotopo |
spin |
abbondanza |
sensibilità |
MHz |
composto |
scala |
|
|
relativa |
assoluta |
||||||
|
H |
|
|
|
|
|
Si(CH3)4 |
Da 12 a 0 |
|
H |
|
1.05 x 10-2 |
9.65 x 10-3 |
1.45 x 10-6 |
|
Si(CD3)4 |
Da 12 a 0 |
|
C |
|
|
1.59 x 10-2 |
1.76 x 10-4 |
|
Si(CH3)4 |
Da 240 a 0 |
|
N |
|
|
1.01 x 10-3 |
1.01 x 10-3 |
|
NH3 |
Da 900 a 0 |
|
N |
|
|
1.04 x 10-3 |
3.85 x 10-6 |
|
NH3 |
Da 900 a 0 |
|
F |
|
|
|
|
|
CFCl3 |
Da 276 a -280 |
|
P |
|
|
6.63 x 10-2 |
6.63 x 10-2 |
|
85% H3PO4 |
Da 270 a -480 |
Fig. 1: Dati di risonanza magnetica nucleare di alcuni nuclei magneticamente attivi.
Le stesse considerazioni possono essere applicate anche al carbonio ricordando che il 12C, isotopo con abbondanza naturale del 99 % circa, ha numero quantico di spin pari a 0 e quindi non ha orientamenti e non è magneticamente attivo. L'isotopo 13C invece ha numero quantico di spin 1/2 come il protone e quindi si comporterà come l'idrogeno dal punto di vista della risonanza magnetica nucleare con alcune importanti differenze.
Innanzitutto l'abbondanza naturale è solo dell'1.1 % e questo significa che solo questa percentuale di nuclei contribuisce alla creazione del segnale NMR. Come conseguenza rispetto all'idrogeno con sensibilità relativa di 1 il carbonio ha una sensibilità relativa molto inferiore come inferiore sarà anche la sensibilità assoluta dato fondamentale per valutare la fattibilità di un esperimento NMR per ogni nucleo. Inoltre, poiché la del carbonio è pari a 6.7, la frequenza di risonanza (quella da applicare per ottenere il segnale) a 4.7 tesla e di 50.3 MHz. Il composto di riferimento è ancora il TMS mentre l'intervallo di osservazione è più ampio e cade nell'intervallo da 0 a 240 ppm.
In termini pratici quindi è facile dedurre che per ottenere uno spettro di risonanza magnetica del carbonio sarà necessario ripetere la sequenza di impulso e acquisizione per un numero superiore di volte rispetto all'idrogeno. Durante l'acquisizione di uno spettro protone la sequenza viene ripetuta normalmente per 16 volte e i FID ottenuti vengono sommati, sottoposti a trasformata di Fourier e infine riportati in forma grafica. Nel caso del carbonio 16 acquisizioni non sono più sufficienti per ottenere un buon rapporto segnale rumore, i picchi cioè non sono più alti della linea di base. Tenendo conto che sperimentalmente l'ampiezza di un segnale NMR è proporzionale circa al cubo della costante giromagnetica la sensibilità dell'esperimento NMR applicato al 13C sarà:
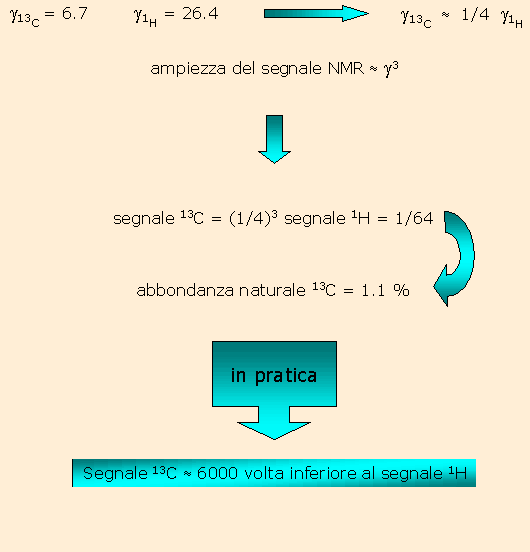
Fig. 2
A causa di queste difficoltà sperimentali la spettroscopia del carbonio si è sviluppata più tardi rispetto a quella del protone ed attualmente con gli strumenti operanti ad elevato campo magnetico è diventata indagine di routine nella determinazione della struttura e della stereochimica di composti organici.
Analisi degli spettri 13C
La bassa abbondanza naturale del 13C rende in teoria molto semplice lo spettro poiché gli accoppiamenti 13C-13C non sono in pratica osservabili in quanto è estremamente improbabile che due nuclei 13C si trovino adiacenti nella stessa molecola. In teoria quindi lo spettro del carbonio dovrebbe essere formato da un insieme di singoletti. In pratica i nuclei del carbonio risentono dello stato di spin degli idrogeni direttamente legati ed i relativi segnali si presentano come doppietti nel caso del CH, come tripletti nel caso del CH2, come quartetti nel caso del CH3 mentre ovviamente sono singoletti i segnali relativi ai carboni quaternari che non hanno idrogeni legati direttamente. A prima vista questa complicazione dello spettro potrebbe sembrare di utilità diagnostica perché permetterebbe di distinguere a prima vista tra carboni primari, secondari ecc. tuttavia poiché le costanti di accoppiamento C-H hanno valori molto elevati spesso le linee relative ai vari segnali sono sovrapposte e lo spettro risulta troppo complicato. Si preferisce in genere acquisire gli spettri del carbonio con la tecnica della doppia risonanza già discussa per il protone. Un canale supplementare irradia alla frequenza di risonanza dell'intero spettro protone annullando gli accoppiamenti con il carbonio. Lo spettro finale quindi sarà effettivamente formato da soli singoletti ognuno dei quali rappresenta un atomo di carbonio a meno di una fortuita coincidenza di spostamento chimico tra due carboni. La spettroscopia del carbonio e del protone si integrano quindi a vicenda ed in particolare con la spettroscopia del carbonio si osserva l'intero scheletro molecolare compresi tutti i gruppi funzionali invisibili al protone quali C=O, C≡N, C=N, C=S.
Spostamenti chimici
Gli spostamenti chimici nella spettroscopia del carbonio sono paralleli, cioè dipendono dagli stessi parametri già individuati per il protone quali ibridazione del carbonio ed elettronegatività del sostituente, anche se si estendono per un maggior numero di ppm da 0 a 240 circa.
Nella tabella seguente vengono riportati in generale gli spostamenti chimici del 13C mentre come nel caso del protone si consiglia l'uso di tabelle più dettagliate reperibili nei più comuni testi che trattano di spettroscopia di risonanza magnetica nucleare.

Fig. 3
A
titolo di esempio analizziamo alcuni spettri reali mentre nella sezione
esercizi sono riportati gli spettri 13C degli stessi composti già
analizzati nell'esercizio 2 della lezione 4.
Facendo riferimento all'aspetto generale degli spettri dobbiamo innanzitutto
notare l'assenza dell'integrale. Nella spettroscopia del carbonio infatti non
esiste più proporzionalità tra l'ampiezza del segnale ed il numero di carboni
che il segnale stesso rappresenta.
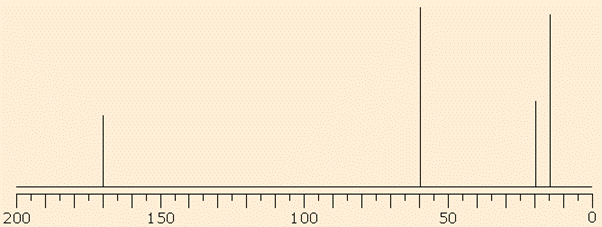
Fig.4: Spettro 13C dell'acetato di etile.
Lo spettro dell'acetato di etile riportato in figura 4 presenta quattro picchi relativi ai quattro carboni presenti nello scheletro molecolare. Alle frequenze più basse, nella parte destra dello spettro, troveremo i carboni ad ibridazione sp3 (più schermati) ed all'interno di questo gruppo gli spostamenti chimici saranno influenzati dall'elettronegatività dei gruppi o atomi adiacenti. Nel caso dell'acetato di etile a 15 ppm troveremo il segnale relativo al metile adiacente al metilene, a 20 ppm il metile adiacente al gruppo carbonilico ed a 60 ppm il segnale relativo al gruppo metilenico che risulta essere il più deschermato in quanto direttamente legato ad un atomo elettronattrattore. Possiamo quindi affermare che il gruppo carbonilico ha un effetto elettronattrattore inferiore all'ossigeno cioè è meno deschermante. Se confrontiamo il 13C ed lo spettro 1H dell'acetato di etile riportato nella figura1 della lezione 3 è possibile notare come esista una stretta analogia tra gli spostamenti chimici osservato per il protone e quelli osservati per il carbonio. Nella parte sinistra dello spettro troveremo i carboni a ibridazione sp2 di tipo etilenico e aromatico (vedere anche la tabella di figura 3). Nel caso dell'acetato di etile in questa zona troveremo il segnale relativo al carbonio del gruppo carbonilico che risuona a frequenze particolarmente elevate (170 ppm) in quanto legato ad un elemento elettronattrattore come l'ossigeno.
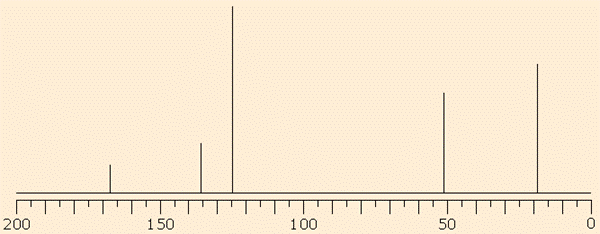
Fig. 5: Spettro 13C del metacrilato di metile.
In figura 5 è riportato lo spettro del metacrilato di metile. Nella zona degli alifatici sono facilmente distinguibili i segnali relativi ai metili: a 18 ppm il segnale del metile legato al carbonio sp2 ed a 50 ppm il segnale più deschermato del metile legato all'eteroatomo. Nella zona dei carboni di tipo etilenico troviamo a 125 ppm il segnale del CH2= ed a 137 ppm il segnale del C=. Come nel caso dell'acetato di etile il segnale a frequenze più alte (167 ppm) va attribuito al C=O.
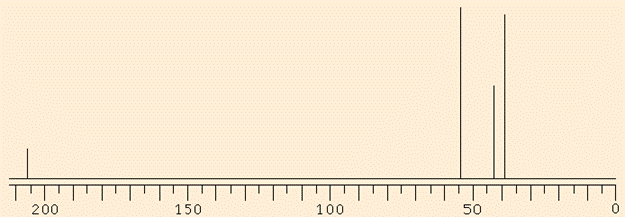
Fig. 6: Spettro 13C dell'N-metil-piperidin-4-one.
In figura 6 è riportato lo spettro dell'N-metil-piperidin-4-one che si differenzia da quelli precedenti per la presenza di carboni equivalenti. I due carboni metilenici adiacenti al gruppo carbonilico sono infatti identici e daranno origine ad un solo segnale così come i due gruppi metilenici adiacenti all'azoto. I carbonio più deschermato è ancora quello del gruppo C=O, mentre nella zona degli alifatici possiamo attribuire il segnale a 55 ppm ai metileni adiacenti all'azoto, mentre è più difficile distinguere i due segnali relativi ai metileni adiacenti al C=O e al metile su azoto. Anche se, come abbiamo già ricordato, non esiste proporzionalità diretta tra numero di atomi di carbonio ed ampiezza del segnale possiamo affermare che il segnale più intenso si riferisce ai due carboni metilenici mentre il meno intenso ad un solo carbonio, quello del metile.
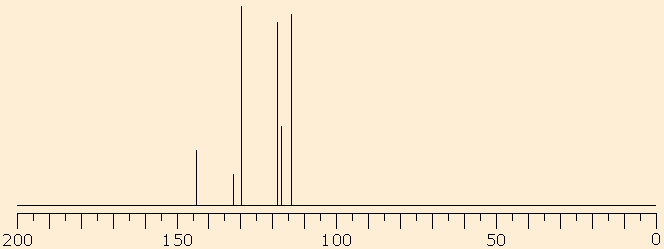
Fig. 7: Spettro 13C della 2,5-dicloro-anilina.
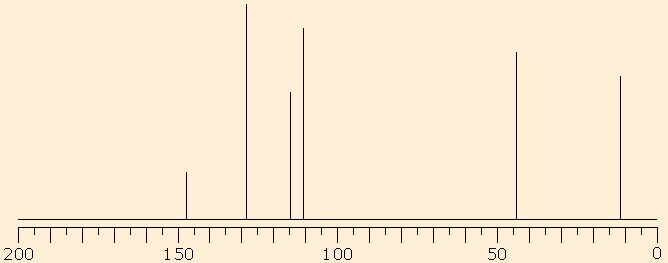
Fig. 8: Spettro 13C della N-etilanilina.
Gli ultimi due spettri si riferiscono a due anelli aromatici. Il primo con sostituzione asimmetrica, la 2,5-dicloro-anilina, presenta nello spettro 6 segnali distinti (Fig. 7), mentre il secondo relativo alla N-etilanilina presenta nella zona degli aromatici quattro segnali in quanto i carboni in orto ed in meta rispetto al sostituente sono equivalenti a due a due (Fig. 8). L'attribuzione dei segnali va fatta in base agli effetti mesomeri ed induttivi dei diversi sostituenti ed esula dagli scopi didattici del corso per biotecnologi.
Come nel caso del protone, oltre all'esperimento fondamentale discusso fino ad ora esistono diversi esperimenti in cui modificando le condizioni di acquisizione è possibile ottenere informazioni supplementari sul composto in esame o facilitare la lettura di spettri complessi. Una delle tecniche più utilzzate prende il nome di APT (Attached Proton Test) in cui una particolare sequenza di acquisizione dello spettro permette di variare la fase del segnale (In positivo od in negativo) a seconda del numero di protoni legato al carbonio. In particolare negli spettri APT i segnali positivi si riferiscono a carboni cui sono legati 2 o 0 idrogeni (gruppi CH2 o carboni quaternari) mentre i segnali negativi si riferiscono a carboni di tipo metilico o metinico (CH3 o CH). Gli spettri riportati nella sezione esercizi sono acquisiti utilizzando la sequenza APT.
 |
| Appunti su: metodi fisici per chimica organica, ferrara metodi fisici appunti, appunti metodi ficidci ctf, https:wwwappuntimaniacomscientifichechimicamodulo-di-metodi-fisici-in-chi93php, |
|
| Appunti Ingegneria tecnico |  |
| Tesine Biologia |  |
| Lezioni Geografia |  |