 |
|
| Appunti scientifiche |
|
 |
|
| Appunti scientifiche |
|
| Visite: 2747 | Gradito: |
Leggi anche appunti:Reazioni di Ossidoriduzione (REDOX)Reazioni di Ossidoriduzione (REDOX) Le reazioni di Ossido-Riduzione servono L'acciaioL'ACCIAIO Il ferro non è più impiegato industrialmente a causa della sua alterabilità La mole ed il Peso molareLa mole ed il Peso molare Un concetto strettamente correlato al peso relativo |
 |
 |
Una reazione si definisce "elementare" quando è costituita da un unico atto reattivo in cui le particelle (atomi, molecole, ioni etc) dei reagenti si urtano per trasformarsi nei prodotti di reazione senza generare nessun intermedio chimico.
Il numero di particelle reagenti che collidono in una reazione elementare è detto molecolarità.
Una reazione unimolecolare (o monomolecolare) è una reazione elementare in cui è coinvolta una sola molecola senza alcun urto. La molecola del reagente si dissocia o isomerizza (si trasforma in un suo isomero). A → P
Una reazione bimolecolare è una reazione elementare in cui sono coinvolte due molecole che collidono fra loro. 2A → P oppure A + B → P. Le reazioni bimolecolari sono di gran lunga le più comuni.
Raramente si possono avere reazioni elementari trimolecolari in cui sono coinvolte tre molecole che collidono fra loro. 3A → P oppure 2A + B → P oppure A + B + C → P
Reazioni di molecolarità superiore non sono note data la bassissima probabilità di un urto contemporaneo tra quattro e più molecole.
La molecolarità di una reazione elementare è quindi definita dalla stechiometria della reazione stessa e coincide con la somma dei coefficienti stechiometrici dei reagenti. Nel caso di reazioni elementari l'ordine complessivo di reazione coincide con la molecolarità e la legge cinetica di una reazione elementare può essere scritta direttamente a partire dall'equazione chimica bilanciata. Ne consegue che in una reazione elementare gli ordini di reazione rispetto ai vari componenti coincidono coi coefficienti stechiometrici
|
Reazione elementare |
Legge cinetica |
Ordine complessivo |
Molecolarità |
|
A → P |
v = k[A] |
|
|
|
2A → P |
v = k[A]2 |
|
|
|
A + B → P |
v = k[A] [B] |
|
|
|
2A + B → P |
v = k[A]2 [B] |
|
|
|
A + B + C → P |
v = k[A] [B] [ C] |
|
|
Ad esempio la reazione 2HI → H2 + I2 è una reazione elementare bimolecolare e quindi la velocità dipende dal quadrato della concentrazione di HI secondo la seguente legge cinetica, direttamente derivabile dalla stechiometria dell'equazione chimica.
![]()
La reazione è dunque di secondo ordine e l'ordine coincide con il valore del coefficiente stechiometrico e con la molecolarità della reazione.
La legge cinetica di una reazione elementare è immediatamente prevedibile. Il problema è che non c'è modo di sapere in anticipo se una data reazione sia o meno elementare e quindi non è possibile assegnare ordine e legge cinetica ad una reazione in via puramente teorica. La legge cinetica va dunque individuata sperimentalmente.
La maggior parte delle reazioni chimiche sono infatti costituite da una successione di reazioni elementari (stadi), ciascuno dei quali genera come prodotti degli intermedi che vengono utilizzati come reagenti nello stadio successivo e che quindi non compaiono come prodotti finali nella reazione complessiva. L'insieme delle reazioni elementari che costituiscono una reazione definiscono il cosiddetto meccanismo di reazione.
Per queste reazioni non ha senso parlare di molecolarità dell'intera reazione, ma di molecolarità di ciascun stadio. Inoltre la legge cinetica, e di conseguenza l'ordine di reazione, non è automaticamente derivabile dalla stechiometria dell'equazione chimica bilanciata.
Come abbiamo detto, la legge cinetica, e quindi l'ordine di reazione, è un dato che va ricavato sperimentalmente studiando la dipendenza della velocità della reazione dalle concentrazioni dei reagenti.
Una volta determinata sperimentalmente la legge cinetica (e l'ordine di reazione) è possibile teorizzare un meccanismo di reazione che sia compatibile con la legge cinetica trovata. Si tenga presente che vi possono essere più meccanismi alternativi, compatibili con la medesima legge cinetica.
Se la reazione avviene in più stadi, la velocità della reazione complessiva (e dunque anche la sua legge cinetica) è condizionata e determinata dalla velocità dello stadio più lento. Tale stadio è definito Stadio cineticamente determinante (Rate Determining Step - RDS) o Stadio cineticamente limitante (Rate Limiting Step - RLS)
Ad esempio, nella reazione NO2 + CO → NO + CO2, si trova sperimentalmente che la velocità dipende dal quadrato della concentrazione di NO2
![]()
La reazione è dunque di secondo ordine e l'ordine non coincide con il coefficiente stechiometrico di NO2 e per di più non risulta nemmeno dipendere dalla concentrazione di CO. Evidentemente non può trattarsi di una reazione elementare ed è dunque necessario ipotizzare un meccanismo di reazione a più stadi.. Il meccanismo accettato per tale reazione è il seguente, costituito da due stadi elementari, ciascuno con la sua molecolarità.
primo stadio 2NO2 → NO3
+ NO In cui è necessario lo scontro di due molecole di NO2
(reazione elementare bimolecolare). Per tale stadio la velocità sarà
dunque ![]() Si forma un
intermedio chimico (NO3) che non compare tra i prodotti della
reazione complessiva e che deve dunque essere consumato come reagente nello
stadio successivo.
Si forma un
intermedio chimico (NO3) che non compare tra i prodotti della
reazione complessiva e che deve dunque essere consumato come reagente nello
stadio successivo.
secondo stadio NO3 + CO → NO2
+ CO2 in cui è necessario lo scontro di una molecola di NO3
con una di CO (reazione elementare bimolecolare). Per tale stadio la velocità
sarà dunque ![]()
Poiché la velocità del primo stadio è molto minore della velocità del secondo stadio, la velocità della reazione complessiva coincide in pratica con la velocità del primo stadio (RDS).
Nel caso in cui lo stadio più lento (RDS) non sia il primo, la derivazione teorica della legge cinetica dal meccanismo di reazione proposto è più complessa.
Ad esempio, la reazione di sintesi del fosgene COCl2 in fase gassosa CO + Cl2 → COCl2 presenta la seguente legge cinetica, sperimentalmente determinata,
v = k [CO] [Cl2]3/2
Per la reazione si accetta il seguente meccanismo in tre stadi, con formazione di radicali (molecole o atomi che possiedono un elettrone spaiato, come ad esempio Cl∙)
Cl2 ![]() 2Cl∙ (equilibrio
veloce)
2Cl∙ (equilibrio
veloce)
Cl∙
+ CO ![]() COCl∙ (equilibrio
veloce)
COCl∙ (equilibrio
veloce)
COCl∙
+ Cl2 ![]() COCl2 + Cl∙ (stadio lento - RDS)
COCl2 + Cl∙ (stadio lento - RDS)
In questo caso la legge cinetica della reazione elementare dello stadio lento, teoricamente assegnata,
v3 = k3 [COCl∙][Cl2]
non risulta congruente con la legge cinetica sperimentalmente determinata per la reazione complessiva, poiché contiene degli intermedi chimici (il radicale COCl∙) che non compaiono ne' tra i reagenti, ne' tra i prodotti della reazione complessiva. Possiamo comunque esprimere le loro concentrazioni in funzione della concentrazione dei reagenti.
Il primo stadio è una reazione elementare unimolecolare, caratterizzata da un equilibrio che si instaura rapidamente tra reagenti e prodotti, quando la velocità v1 della reazione diretta
v1 = k1 [Cl2]
eguaglia la velocità v-1 della reazione inversa
v-1 = k-1 [Cl∙]2
essendo dunque v1 = v-1, possiamo eguagliare anche i secondi membri ed esplicitare la concentrazione di Cl∙
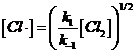
Il secondo stadio è una reazione elementare bimolecolare, caratterizzata da un equilibrio che si instaura rapidamente tra reagenti e prodotti, quando la velocità v2 della reazione diretta
V2 = k2 [Cl∙][CO]
eguaglia la velocità v-2 della reazione inversa
v-2 = k-2 [COCl∙]
essendo dunque v2 = v-2, possiamo eguagliare anche i secondi membri ed esplicitare la concentrazione di COCl∙
2) ![]()
sostituiamo ora nella relazione 2) la concentrazione del radicale Cl∙ trovata nella 1), ottenendo
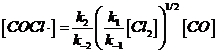
Il terzo stadio è lo stadio cineticamente determinante (RDS), costituito da una reazione elementare bimolecolare la cui velocità v3 condiziona la velocità complessiva della reazione (v3 ≈ v)
v3 = k3 [COCl∙][Cl2]
sostituiamo ora nella 4) la concentrazione dell'intermedio chimico COCl∙, con la il risultato della 3) in cui la concentrazione dell'intermedio è espressa in funzione delle concentrazioni dei reagenti (CO e Cl2)
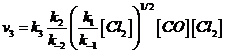
ed in definitiva
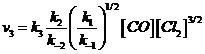
che risulta ora perfettamente consistente con la legge cinetica
sperimentalmente determinata. E dunque
la costante cinetica k, trovata
sperimentalmente per la reazione complessiva, coincide con la costante cinetica
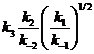 teoricamente calcolata, espressa in funzione
delle costanti cinetiche dei singoli stadi.
teoricamente calcolata, espressa in funzione
delle costanti cinetiche dei singoli stadi.
 |
| Appunti su: molecolaritC3A0 reazione chimica, ordjne nelle reazioni bimolecolari, |
|
| Appunti Biologia |  |
| Tesine Ingegneria tecnico |  |
| Lezioni Geografia |  |