 |
|
| Appunti scientifiche |
|
 |
|
| Appunti scientifiche |
|
| Visite: 13310 | Gradito: |
Leggi anche appunti:Prodotti di solubilità (ordinati per catione) (a 25°C)Prodotti di solubilità (ordinati per catione) (a 25°C) AgOH Composti complessi e agenti complessantiComposti complessi e agenti complessanti Sali e acidi complessi appartengono Il Processo DryIl Processo Dry Il primo processo di realizzazione della doppia giunzione |
 |
 |
Gli enantiomeri hanno proprietà fisiche identiche (p. ebollizione, p. fusione, solubilità etc), ad eccezione dell'attività ottica e proprietà chimiche identiche, con l'esclusione della interazione con reattivi chirali (otticamente attivi).
Si definisce attività ottica la capacità di una molecola di ruotare il piano della luce polarizzata. In particolare quando una luce polarizzata, che vibra lungo un solo piano, attraversa una soluzione contenente una molecola chirale il suo piano di vibrazione viene ruotato di un certo angolo [] che dipende dalla concentrazione, dalla lunghezza d'onda della luce monocromatica, dalla temperatura, dal solvente usato e dalla lunghezza del percorso ottico.
Per standardizzare i valori delle
attività ottiche si è adottata come unità di misura la rotazione specifica (o potere rotatorio specifico) ![]() misurata ad una certa temperatura (in genere t = 25° C) e ad
una certa lunghezza d'onda (in genere =
589 nm
riga D dello spettro di emissione del sodio)
misurata ad una certa temperatura (in genere t = 25° C) e ad
una certa lunghezza d'onda (in genere =
589 nm
riga D dello spettro di emissione del sodio)
![]() :
:

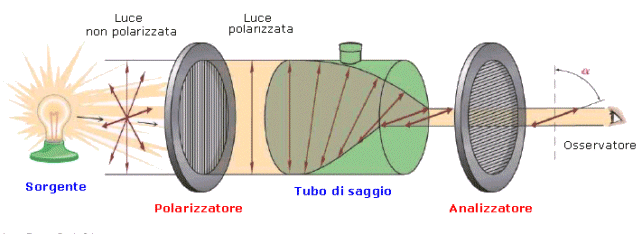
La misura dell'attività ottica è molto comune e serve a distinguere gli enantiomeri fra di loro. Due enantiomeri hanno infatti, a parità di condizioni, la medesima rotazione specifica (ruotano il piano della luce polarizzata del medesimo angolo), ma di segno opposto. L'enantiomero che produce una rotazione in senso orario (destrogiro) viene indicato con il segno (+), mentre quello che produce una rotazione in senso antiorario (levogiro) con il segno (-). I due enantiomeri vengono anche definiti antipodi ottici. Un sistema contenente un ugual numero di molecole dei due enantiomeri non presenta attività ottica, viene contraddistinto dal simbolo (±) posto davanti al nome del composto e si definisce miscela racemica.
Una miscela in cui uno dei due enantiomeri è presente in maggiore quantità mostrerà una rotazione ottica proporzionale alla percentuale della specie in eccesso.
La percentuale dell'enantiomero in eccesso viene detta eccesso enantiomerico ed è calcolata come rapporto percentuale tra la rotazione misurata per la miscela in esame ed il potere rotatorio specifico dell'enantiomero puro.
![]()
Una volta determinato l'eccesso enantiomerico è possibile risalire alle proporzioni dei due enantiomeri nella miscela pari rispettivamente a (100+ e.e%)/2 e (100-ee%)/2.
Una miscela racemica non può essere separata dai suoi componenti mediante i comuni metodi fisici (cristallizzazione, distillazione etc.). Per la separazione si deve prevedere l'uso di specie chirali che interagiscono diversamente con le due molecole di differente chiralità. Nei sistemi biologici, ad esempio, questo ruolo è svolto dagli enzimi che sono in grado di metabolizzare una forma enantiomerica lasciando l'altra inalterata.
Il metodo più usato nei laboratori chimici per la separazione degli enantiomeri o, come si suole dire, per la risoluzione di una miscela racemica, consiste nel trasformare, per reazione con un reagente chirale, gli enantiomeri in composti achirali che possiedono proprietà fisiche diverse.
La stereogenicità è la proprietà che possiede una struttura atomica, per questo detta struttura stereogenica, di produrre un nuovo stereoisomero come conseguenza dello scambio tra due atomi (o gruppi chimici) ad essa legati (inversione). Le strutture stereogeniche (o elementi stereogenici) possono rendere chirali e quindi otticamente attive le molecole in cui si trovano.
La presenza di una struttura stereogenica non rende automaticamente chirale una molecola.
Sono strutture stereogeniche i centri stereogenici, gli assi stereogenici ed i piani stereogenici, spesso impropriamente detti centri chirali, assi chirali e piani chirali.
L'aggettivo "chirale" andrebbe infatti usato per indicare l'intera molecola (ovviamente se essa è chirale) e non una parte di essa. La chiralità è infatti una proprietà dell'intera molecola e non di un atomo o di un gruppo di atomi al suo interno.
Se una molecola risulta chirale come conseguenza della presenza di una di queste strutture stereogeniche, allora si parla di chiralità centrale, chiralità assiale e chiralità planare, Esistono infine molecole chirali come conseguenza di una struttura elicoidale. La chiralità elicoidale è anche detta elicità.
La chiralità centrale si presenta quando un gruppo di sostituenti sono legati ad un atomo centrale (centro stereogenico o stereocentro o, impropriamente, centro chirale) in modo da formare una molecola che non è sovrapponibile alla sua immagine speculare.
Lo stereocentro di gran lungo più diffuso è l'atomo di carbonio tetraedrico asimmetrico, un carbonio ibridato sp3 tetrasostituito (legato a 4 gruppi chimici uno diverso dall'altro). L'atomo di carbonio asimmetrico è spesso individuato con un asterisco ad apice (C*). Esistono tuttavia stereocentri tetraedrici non carboniosi (Azoto, Zolfo, Fosforo etc) e sono inoltre possibili stereocentri non tetraedrici, particolarmente diffusi nei composti di coordinazione (complessi)
Stereocentri tetraedrici
L'aldeide glicerica è un esempio di molecola chirale per la presenza in essa di un centro stereogenico (carbonio asimmetrico C*). Per rappresentare molecole che possiedono centri stereogenici (in particolare monosaccaridi) sono spesso utilizzate Le proiezioni di Fischer. Nel proiettare una molecola contenente un solo stereocentro la catena più lunga di atomi di carbonio deve essere riportata verticalmente, collocando in alto il carbonio al quale spetta il più basso numero di posizione derivante dalla nomenclatura IUPAC.
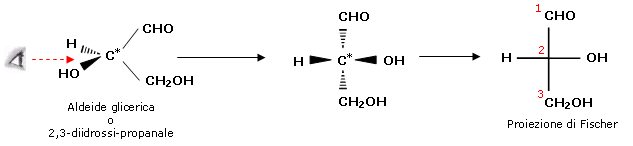
I 4 sostituenti devono infine essere disposti in modo tale che i legami verticali si allontanino dall'osservatore uscendo dietro il piano del foglio, mentre i legami orizzontali si avvicinino all'osservatore uscendo davanti al piano del foglio.
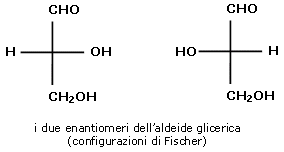
Per verificare la sovrapponibilità di due proiezioni di Fischer è necessario far scivolare le molecole facendole rimanere sempre sul piano del foglio.
Se le due proiezioni sono sovrapponibili, si tratta della stessa molecola.
I due enantiomeri di una molecola chirale differiscono solamente per la disposizione spaziale dei loro sostituenti intorno alla struttura stereogenica. Presentano cioè una diversa configurazione. L'attività ottica di molti prodotti naturali, in particolare quella degli zuccheri, era nota ai chimici già nel XIX secolo ma per oltre cent'anni la determinazione della configurazione assoluta risultò un problema di non semplice soluzione. Non esiste infatti alcuna correlazione tra la configurazione degli enantiomeri ed il senso in cui ruotano il piano della luce polarizzata. Per esempio, lo zucchero otticamente attivo più semplice, il 2,3-diidrossipropanale, comunemente chiamato gliceraldeide, ha un solo stereocentro ed esiste come coppia di enantiomeri, la (+)-gliceraldeide e la (-)-gliceraldeide. Non c'è alcun modo diretto per associare i due enantiomeri alle due strutture di Fischer che li rappresentano.
In altre parole, la reale disposizione degli atomi legati allo stereocentro, che corrisponde alla configurazione assoluta di un composto, non può essere assegnata sulla base del segno del potere rotatorio.
Si decise quindi arbitrariamente di assegnare la configurazione ai due enantiomeri della gliceraldeide, associando alla gliceraldeide destrogira la proiezione con l'ossidrile in C* posto a destra e definendola pertanto D, mentre alla gliceraldeide levogira la proiezione di Fischer con l'ossidrile in C* posto a sinistra e definendola pertanto L. Si noti che D ed L definiscono la posizione dell'ossidrile legato al carbonio asimmetrico e non il senso di rotazione del piano della luce polarizzata
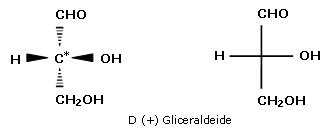
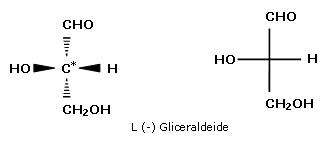
La scelta aveva ovviamente una probabilità su due di essere corretta. Quando nel 1951 J.M.Bijvoet determinò sperimentalmente tramite diffrazione a raggi X la configurazione assoluta dell'acido (-)-tartarico, precedentemente correlata alla configurazione della (+)-Gliceraldeide, trovò che le configurazioni dei due enantiomeri della gliceraldeide erano state assegnate correttamente.
D ed L rappresentano una coppia di descrittori stereochimici (o stereodescrittori) di configurazione relativa.
Mediante processi di conversione chimica è infatti possibile stabilire il rapporto di configurazione tra due composti otticamente attivi, trasformando un composto nell'altro tramite reazioni che non implicano la rottura di un legame di un centro chirale. anche senza conoscerne la configurazione assoluta. La configurazione di un composto chirale resta infatti inalterata a meno che non venga rotto almeno uno dei legami dello stereocentro.
Così ad esempio è possibile partendo dalla D(+) gliceraldeide ottenere mediante sintesi chimica, l'acido (-)-tartarico che è l'acido tartarico meno abbondante in natura. Così facendo si è assegnata all'acido tartarico levogiro la configurazione relativa D(-)-tartarico. In questo modo sono state stabilite le configurazioni relative di un grande numero di composti organici.
Si noti come non esista alcuna relazione generale tra la configurazione D ed L di una molecola ed il segno (+) e (-) del suo potere rotatorio. Certi composti appartenenti alla serie sterica D sono levogiri e viceversa.
Per gli amminoacidi l'attribuzione degli stereodescrittori D/L prevede che venga considerato, nella proiezione di Fischer, il gruppo amminico legato al primo atomo di carbonio asimmetrico. Se il gruppo amminico è a destra, l'amminoacido appartiene alla serie D, se è a sinistra appartiene alla serie L. L'alanina naturale è l'acido (2S)-2-aminopropanoico ed è un amminoacido appartenente alla serie L.
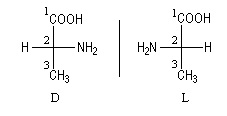
Le tecniche di difrattometria a raggi X hanno successivamente permesso di stabilire la configurazione assoluta di un composto chirale senza doverla correlare ad altri composti. Sono stati perciò introdotti gli stereodescrittori di configurazione assoluta R ed S.
Per assegnare univocamente il nome e la configurazione assoluta degli enantiomeri si ricorre alle regole di Cahn-Ingold-Prelog (già viste nel capitolo dedicato all'isomeria geometrica) che permettono di descrivere la configurazione di uno stereocentro definendola rispettivamente R (dal latino rectus, quindi "destrorsa") o S (dal latino sinister, quindi "sinistrorsa") in base all'ordine con cui i differenti sostituenti sono disposti intorno allo stereocentro.
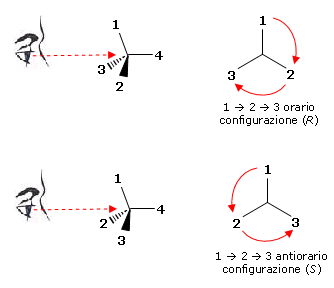
Una volta che la priorità CIP sia stata assegnata ai gruppi legati allo stereocentro, si orienta la molecola in modo tale che il sostituente a più bassa priorità (4) sia diretto lontano dall'osservatore, mentre i gruppi a priorità più elevata (1,2,3) siano rivolti verso l'osservatore. A questo punto, se per andare ordinatamente dal gruppo a priorità maggiore a quello a priorità minore (1 3) si procede in senso orario, si assegna allo stereocentro la configurazione R. Se, invece, si procede in senso antiorario, si assegna allo stereocentro la configurazione S. Si scrive R ed S in corsivo (italico) e non R ed S
Assegniamo la configurazione assoluta alla D(+)-Gliceraldeide
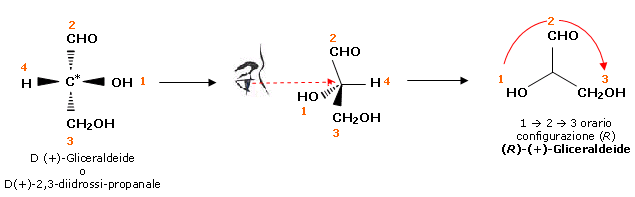
E' evidente che manipolare correttamente le formule spaziali rimanendo sul piano del foglio non è sempre agevole. La stessa operazione può essere condotta più facilmente sulle proiezioni di Fischer, a patto di osservare però le seguenti regole:
1) si stabilisce la priorità tra i quattro gruppi legati al centro chirale come già fatto in precedenza;
2) ci si assicura che il gruppo a minore priorità (4) sia posto in una delle due posizioni verticali della croce di Fischer (in tal modo si è certi che esso si trova dietro il piano del foglio e quindi lontano dall'osservatore);
3) soddisfatte le prime due condizioni, se per passare dal gruppo 1 al 2 al 3 il senso di rotazione è orario, allora la configurazione assoluta è R. Se invece il senso è antiorario la configurazione è S;
4) se il gruppo a minore priorità si trova su uno dei bracci orizzontali (cioè in posizione non corretta perché vicina all'osservatore), prima di assegnare la configurazione (cioè prima di andare al punto 3) è necessario modificare opportunamente la proiezione di Fischer. Le proiezioni di Fischer non sono liberamente modificabili, in quanto alcune trasformazioni lasciano la configurazione inalterata, altre portano alla configurazione dell'enantiomero. Si tenga presente che:
a) Un numero dispari di scambi di due qualsiasi sostituenti comporta l'inversione della configurazione dello stereocentro con formazione dell'enantiomero. Un numero pari di scambi di due qualsiasi sostituenti lascia invece inalterata la configurazione dello stereocentro.
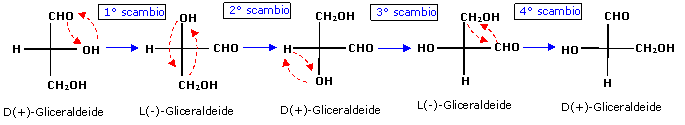
b)
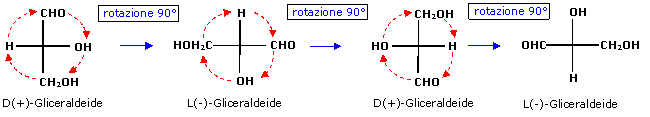 Ogni
rotazione di 90° trasforma la
configurazione in quella del suo enantiomero. Se ne deduce che una rotazione di
180° lascia inalterata la configurazione dello stereocentro
Ogni
rotazione di 90° trasforma la
configurazione in quella del suo enantiomero. Se ne deduce che una rotazione di
180° lascia inalterata la configurazione dello stereocentro
c) Tenendo fermo un sostituente qualsiasi e ruotando gli altri tre si lascia inalterata la configurazione dello stereocentro
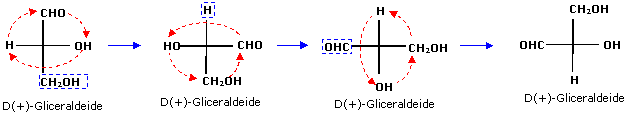
Proviamo allora ad assegnare la configurazione assoluta alla seguente proiezione di Fischer che rappresenta la D(+)-Gliceraldeide.

Poiché il gruppo a minor priorità (H) si trova su di un braccio orizzontale, modifichiamo la proiezione di Fischer, mantenendo costante la configurazione, usando entrambi i metodi proposti.
1° Metodo: doppio scambio
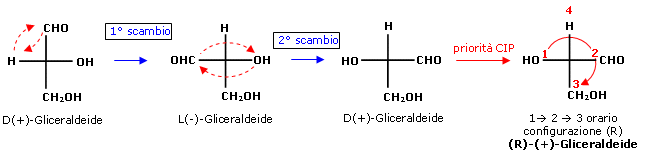
2° metodo: rotazione 3 sostituenti
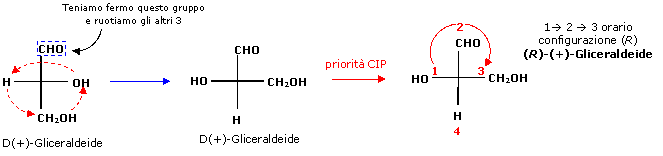
Nota: se il gruppo a minor priorità si trova in una posizione orizzontale è comunque possibile assegnare la configurazione assoluta allo stereocentro, senza modificare la proiezione di Fischer. E' sufficiente ricordare che in tal caso il senso di rotazione trovato per i primi 3 sostituenti va invertito.
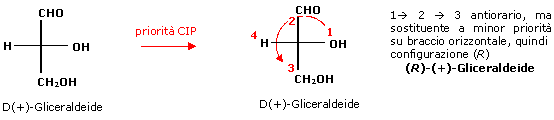
Si noti ancora una volta che l'assegnazione della configurazione assoluta di un composto come R o S non ha niente a che vedere con il segno della rotazione, per stabilire il quale è invece necessaria una misura sperimentale del potere rotatorio specifico
Le miscele racemiche vengono precedute dal prefisso (RS)
La configurazione assoluta di una molecola con più di uno stereocentro non comporta particolari problemi. E' necessario considerare separatamente ciascun centro chirale ed assegnargli la configurazione R o S accompagnata da un numero che indichi a quale atomo della catena la configurazione si riferisce. Le formule seguenti, ad esempio, sono quelle dei due enantiomeri dell'acido tartarico o acido (2R,3R)-2,3-diidrossibutan-1,4-dioico e acido (2S,3S)-2,3-diidrossibutan-1,4-dioico.
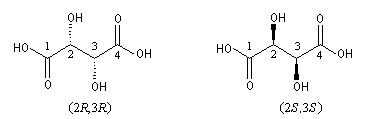
L'assegnazione della configurazione assoluta si effettua più facilmente utilizzando le proiezioni di Fischer, ricordando naturalmente che i punti di intersezione tra le linee rappresentano gli stereocentri, che le valenze verticali rappresentano i legami diretti dietro il foglio, lontano dall'osservatore, e quelle orizzontali i legami rivolti verso l'osservatore. Una proiezione di Fischer rappresenta quindi la molecola nella sua conformazione eclissata.
Volendo ad esempio trasformare una proiezione a cavalletto sfalsata di uno degli stereoisomeri dell'acido tartarico in una proiezione di Fischer, si dovranno effettuare le seguenti operazioni. Si ruoti la molecola intorno al legame semplice C2-C3 fino a disporla in una conformazione eclissata. Si collochi la catena lineare più lunga lontano dall'osservatore e si proietti la molecola sul piano, ricordando di disporre l'atomo di carbonio C1 in alto.
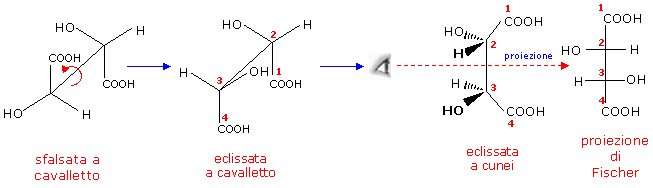
Esempio
Assegniamo la configurazione assoluta ai due stereocentri C2 e C3 del 2-Bromo-3-idrossi-butano. Ricordando che tutti i legami orizzontali devono puntare verso l'osservatore si ottiene
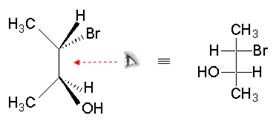
N a b c Si consideri ora uno stereocentro per volta e si modifichino le proiezioni di Fischer in modo da portare il sostituente a minor priorità in posizione verticale.
Iniziamo dall'atomo di carbonio asimmetrico in C2. Essendo l'atomo di Idrogeno il sostituente a minor priorità lo portiamo in posizione verticale
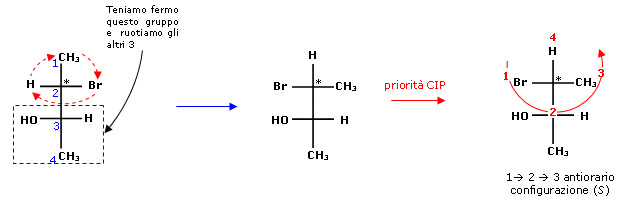
Ora assegniamo la configurazione allo stereocentro in C3. Ancora una volta dobbiamo portare l'atomo di Idrogeno, il sostituente a minor priorità, in posizione verticale
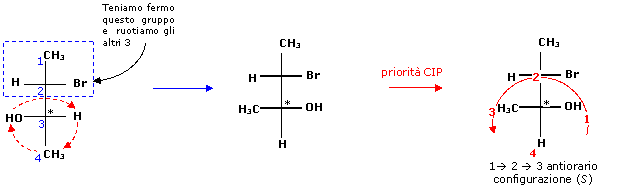
Il composto è dunque (2S,3S)-3-Bromo-2-butanolo
In generale un composto con n stereocentri presenta un massimo di 2n = S stereoisomeri, che formano (S-1)S/2 coppie di isomeri di cui S/2 coppie di enantiomeri e (S-2)S/2 coppie di diastereoisomeri. Ad esempio con 2 stereocentri esistono S=4 possibili stereoisomeri: (2S, 3R), (2R, 3S), (2S, 3S) e (2R, 3R). Di questi le S/2 = 4/2 = 2 coppie che presentano tutte le configurazioni degli stereocentri tra loro invertite sono enantiomeri, mentre le rimanenti (S-2)S/2 = (4-2)4/2 = 4 coppie sono diastereoisomeri, secondo lo schema seguente
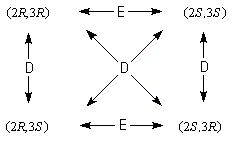
La notazione di Fischer è particolarmente utile per assegnare la configurazione assoluta a molecole con più stereocentri. Consideriamo ad esempio il monosaccaride aldopentoso o 2,3,4,5-tetraidrossipentanale che possiede 3 stereocentri in C2, C3 e C4. Ci aspettiamo un massimo di 23 = 8 stereoisomeri suddivisi in 8/2 = 4 coppie di enantiomeri.
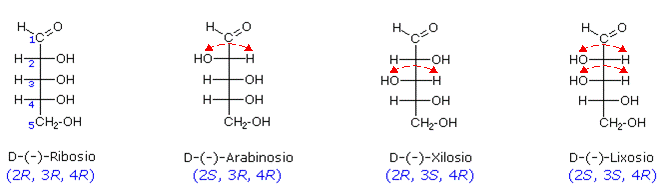 Tenendo ferma la configurazione dello stereocentro in C4 (R
nell'esempio) e invertendo ordinatamente la configurazione degli altri
stereocentri si ottengono i 4 diastereoisomeri della serie D (hanno tutti
l'ossidrile sull'ultimo stereocentro a destra)
Tenendo ferma la configurazione dello stereocentro in C4 (R
nell'esempio) e invertendo ordinatamente la configurazione degli altri
stereocentri si ottengono i 4 diastereoisomeri della serie D (hanno tutti
l'ossidrile sull'ultimo stereocentro a destra)
Ciascuno di questi
4 diastereoisomeri ha un enantiomero della serie L, che si può facilmente
costruire invertendo le configurazioni di tutti gli stereocentri di ciascun
isomero. 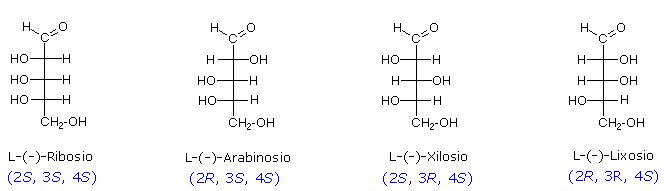
Le 4 coppie di enantiomeri sono dunque le seguenti
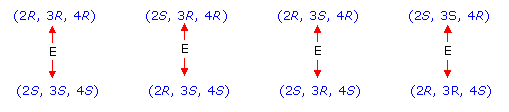
Le rimanenti (S-2)S/2 = (8-2)8/2= 24 coppie sono coppie di diastereoisomeri
La configurazione di composti racemici con più di uno stereocentro viene descritta utilizzando la notazione RS per ciascun stereocentro. Così una soluzione racemica di D-Ribosio verrà indicata come (2RS, 3RS 4RS), mentre una soluzione racemica di D-Arabinosio verrà indicata come (2SR, 3RS 4RS).
Si definiscono epimeri due diastereoisomeri che, avendo due o più stereocentri, differiscono solo per la configurazione di uno solo di essi. Così, ad esempio, Il Ribosio e l'Arabinosio sono epimeri in C2, l'Arabinosio e lo Xilosio sono epimeri in C3. Ma l'Arabinosio ed il Lixosio non sono epimeri perché hanno configurazione diversa sia in C2 che in C3.
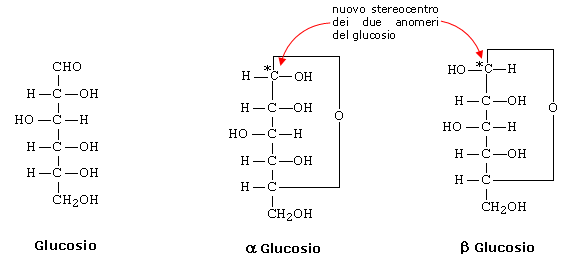
Un tipo particolare di epimeri sono gli anomeri. Gli anomeri si formano nei monosaccaridi con più di quattro atomi di carbonio, i quali tendono ad assumere forme cicliche a causa della tendenza del penultimo ossidrile a reagire con il gruppo carbonile, con formazione di un semiacetale. Nella forma ciclica il primo atomo di carbonio diventa un nuovo centro chirale, dando luogo a due nuovi diasteroisomeri che si differenziano per la configurazione di questo centro detti appunto anomeri.
I due anomeri si distinguono con le lettere greche a e b. Con a è designato l'anomero che diminuisce il proprio potere rotatorio nel fenomeno della mutarotazione e con b quello che l'aumenta.
In certi casi il numero di stereoisomeri è inferiore al numero totale possibile. Il caso più frequente si presenta con i composti meso. Un composto meso è una molecola con 2 o più centri chirali, che presenta tuttavia un'immagine speculare ad essa sovrapponibile e risulta pertanto achirale ed otticamente inattiva. Per riconoscere un composto meso in una proiezione di Fischer è sufficiente controllare che la metà superiore della molecola sia l'immagine speculare della metà inferiore. Un esempio di composto meso si ha con l'acido mesotartarico.
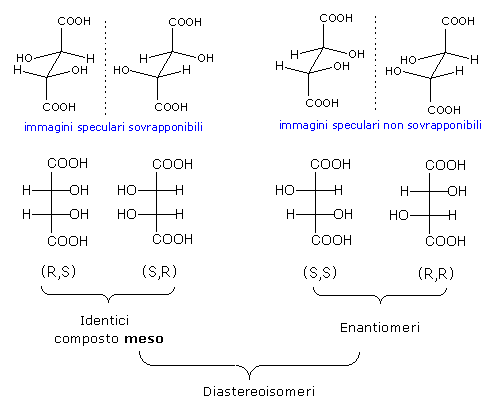
Si noti come il composto (R,S) ed il composto (S,R) siano in realtà identici e costituiscano un unico composto denominato acido mesotartarico. Ognuna delle due formule di Fischer che rappresenta L'acido mesotartarico presenta un piano ideale che la taglia a metà in modo tale che la metà superiore della molecola è l'immagine speculare della metà inferiore.
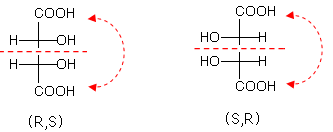
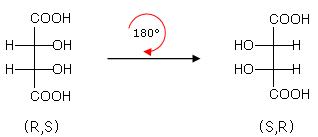
Si noti inoltre che ruotando di 180° la formula di Fischer del composto (R,S) (rotazione permessa, che lascia inalterata la configurazione assoluta del composto) si ottiene il composto (S,R)
L'acido mesotartarico, come tutti i composti meso, è otticamente inattivo per compensazione intramolecolare. Infatti i due centri chirali presenti nella stessa molecola, essendo identici ma con configurazione opposta, ruotano il piano della luce polarizzata dello stesso valore ed in senso opposto.
Nel caso dell'acido mesotartarico, che possiede due stereocentri, non esistono dunque 22=4 stereoisomeri, ma solo 3 stereoisomeri, poiché gli isomeri (R,S) ed (S,R) sono in realtà un unico composto meso.
Nel caso invece dell'acido 2,3,4,5-tetraidrossiesandioico (acido glucarico), che possiede 4 stereocentri, sono possibili un massimo di 24=16 stereoisomeri, ma esistono solo 14 stereoisomeri, poiché due coppie di diastereoisomeri costituiscono due composti meso.
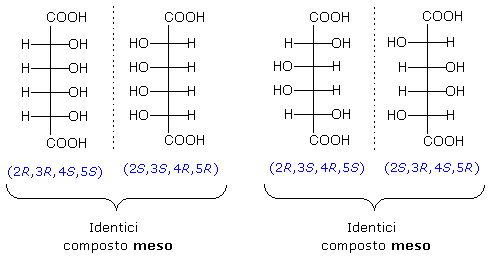
Se il composto meso è
formato da un numero dispari di atomi di carbonio, allora il piano che divide
la molecola in due parti speculari passa per l'atomo di carbonio centrale. E'
semplice verificare che tale atomo non è in linea di principio
asimmetrico in quanto presenta due sostituenti identici. 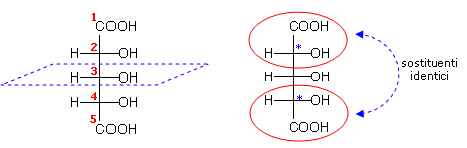
In realtà anche l'atomo di carbonio centrale può presentare una sorta di asimmetria in quanto i due sostituenti identici possono presentarsi con configurazioni opposte: R ed S oppure S ed R. In questo caso l'atomo centrale è detto pseudosimmetrico e la sua configurazione è connotata con le lettere minuscole r ed s. Per assegnare la configurazione all'atomo pseudosimmetrico è necessario ricordare che, per le regole CIP, un sostituente con configurazione R ha precedenza su di un sostituente con configurazione S.
L'acido 2,3,4-triidrossipentandioico (acido arabinarico), ad esempio, presenta quattro stereoisomeri: una coppia di enantiomeri con atomo centrale achirale e due forme meso con atomo centrale pseudosimmetrico.
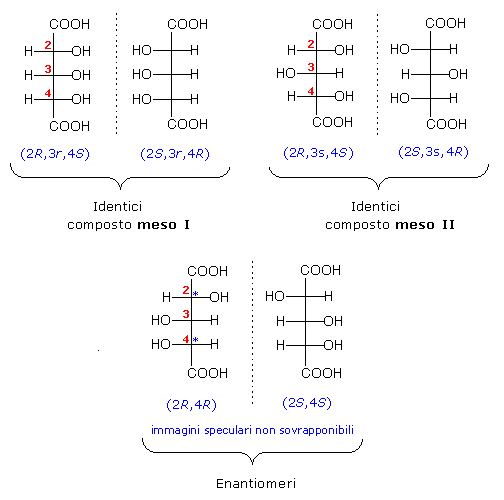
Si noti come invertendo la configurazione del carbonio centrale C3 del primo composto meso (3r 3s) si ottenga il secondo composto meso.
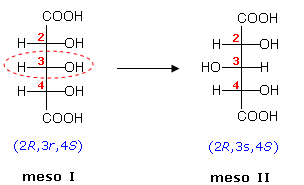
Se invece invertiamo la configurazione del carbonio C3 (che non è stereogenico) in uno dei due enantiomeri, otteniamo il medesimo enantiomero. Per verificarlo è sufficiente ruotare la formula di Fischer di 180°, come mostrato nella figura seguente
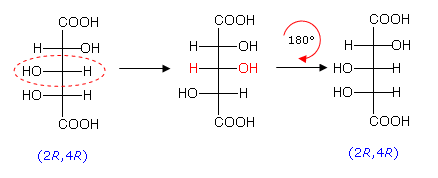
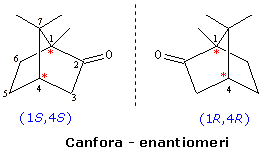
In certi casi il numero degli stereoisomeri è inferiore al numero massimo possibile anche per cause diverse dalla presenza di molecole achirali come i composti meso. E' ad esempio possibile che alcune configurazioni siano rese impossibili da impedimenti di tipo sterico. Un tipico esempio si ha con i sistemi 'a ponte'. Vengono definiti sistemi a ponte i sistemi ciclici fusi attraverso atomi non-adiacenti. Nella canfora o 1,7,7-trimetilbiciclo[2,2,1]eptan-2-one, ad esempio, i due atomi di carbonio 'testa di ponte' (C1 e C4) sono chirali. Nonostante possieda due stereocentri, la canfora presenta solo due stereoisomeri, tra loro enantiomeri, con configurazione (1R,4R) e (1S,4S). Data la rigidità della struttura a ponte, non è infatti possibile invertire la configurazione di un solo stereocentro, mantenendo l'altro inalterato. Non esistono quindi gli stereoisomeri con configurazione (1R,4S) ed (1S,4R).
Come abbiamo già vista nel caso degli stereodescrittori D/L, la configurazione relativa è la configurazione di uno stereocentro correlata a quello di un'altra molecola o, come vedremo ora, ad un altro stereocentro della medesima molecola. In alcuni casi, come ad esempio quando si presentano solo due stereocentri, può essere più utile conoscere la configurazione relativa di uno stereocentro rispetto ad un altro, piuttosto che la sua configurazione assoluta.
Gli stereodescrittori di configurazione relativa like/unlike si applicano spesso a molecole con due stereocentri.
Se i due stereocentri presentano lo stesso descrittore di configurazione assoluta, entrambi R o entrambi S, allora lo stereoisomero è definito like (indicato anche l o R*R*)
Se i due stereocentri presentano descrittore diversi di configurazione assoluta, R,S o S,R allora lo stereoisomero è definito unlike (indicato anche u o R*S*)
Gli enantiomeri (R, R) ed (S, S) formano la coppia like
Gli enantiomeri (R, S) ed (S, R) formano la coppia unlike
L'esempio seguente riguarda i quattro stereoisometri dell'aldotetroso
|
Coppie |
|
|
|
Composto |
Eritrosio |
Treosio |
|
Notazione |
like |
unlike |
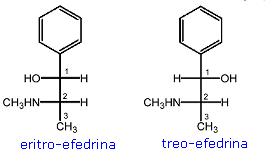
Gli stereodescrittori like/unlike dovrebbero sostituire, secondo quanto consigliato dall'IUPAC, la vecchia nomenclatura eritro/treo, mutuata dalla chimica dei carboidrati ed in particolare proprio dagli stereoisomeri del 2,3,4-triidrossibutanale, i quali vengono raggruppati in due coppie di enantiomeri chiamate rispettivamente eritrosio e treosio.
Si usa il prefisso eritro per i composti che derivano dall'Eritrosio o che, comunque, presentino una disposizione analoga dei sostituenti sui due atomi di carbonio asimmetrici. Si usa il prefisso treo per i composti che derivano dal Treosio o che, comunque, presentino una disposizione analoga dei sostituenti sui due atomi di carbonio asimmetrici
Se si usano le proiezioni di Fischer è facile vedere come i composti eritro abbiano i due sostituenti a maggior priorità (regole CIP) dalla medesima parte dell'asse verticale che rappresenta la catena carboniosa, mentre i composti treo presentino i due sostituenti a maggior priorità da parti opposte.
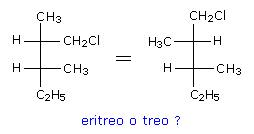
La notazione eritro/treo si presta ad interpretazioni ambigue, in particolare per quel che riguarda la scelta della catena carboniosa principale. Si vedano ad esempio le due proiezioni di Fischer equivalenti della molecola seguente
Le proiezioni di Fischer sono particolarmente utili per confrontare le configurazioni di stereoisomeri appartenenti a famiglie di composti correlati, come ad esempio i carboidrati. Tuttavia la conformazione eclissata della molecola che sta alla base della proiezione di Fischer è poco realistica e quando si rappresentano composti contenenti 2 o più stereocentri, molti chimici preferiscono usare una rappresentazione a zig-zag per la catena carboniosa principale, con i sostituenti degli stereocentri connessi con legami a cuneo.
La catena carboniosa principale a zig-zag giace sul piano del foglio, mentre i sostituenti si trovano sopra o sotto il piano. Con tale rappresentazione spesso si usano gli stereodescrittori di configurazione relativa sin/anti, mutuati dalla notazione utilizzata nei composti bicilici.
Se i due sostituenti a maggior priorità di due atomi di carbonio asimmetrici si trovano dal medesimo lato del piano individuato dalla catena carboniosa principale, i due stereocentri si trovano in una configurazione relativa sin, mentre se giacciono su lati opposti si trovano in configurazione anti.
|
|
|
|
|
|
sin |
sin |
anti |
anti |
Si noti come la notazione eritro/treo corrisponda alla notazione sin/anti (treo = sin e eritro = anti). Tuttavia la posizione dei due sostituenti a maggior priorità rispetto alla catena carboniosa principale è diversa in una proiezione di Fischer rispetto ad una proiezione a cunei, potendo così generare confusione.
Si confrontino ad esempio le diverse proiezioni del 2,3-diclorobutano. Nel composto treo la proiezione a cunei porta i due sostituenti maggiori (Cloro) dalla medesima parte del piano del foglio, mentre la formula di Fischer li porta su lati opposti della catena. Nel composto eritro la proiezione a cunei porta i due sostituenti da parti opposte del piano del foglio, mentre la formula di Fischer li porta sul medesimo lato della catena.
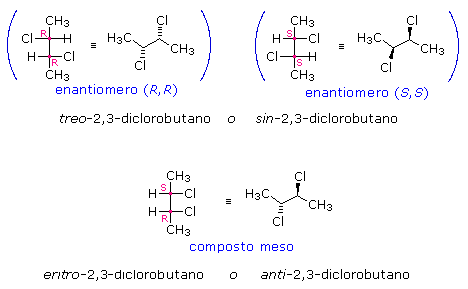
Si noti come le configurazioni sin(treo)/anti(eritro) non siano a priori correlabili con le configurazioni like/unlike. Una configurazione sin può essere sia like che unlike.

La nomenclatura sin/anti viene spesso utilizzata per descrivere la configurazione relativa di composti aciclici con più di due stereocentri. Il centro stereogenico più vicino al primo carbonio della catena principale (C1) serve come riferimento. Gli altri stereocentri presenteranno rispetto ad esso una disposizione sin o anti.
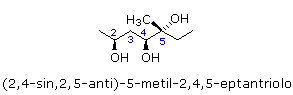
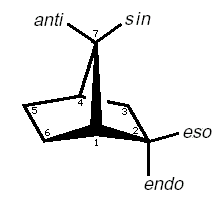
La gli stereodescrittori di configurazione relativa sin/anti ed eso/endo vengono anche utilizzati per definire l'orientazione di sostituenti legati ad atomi di carbonio situati tra due atomi 'testa di ponte' in sistemi biciclici fusi.
I sostituenti legati all'anello a più bassa numerazione (anello più grande) usano gli stereodescrittori eso/endo.
Eso = sostituente orientato verso l'anello a più alta numerazione (anello più piccolo)
Endo = sostituente orientato dalla parte opposta
I sostituenti legati all'anello a più alta numerazione (anello più piccolo) usano gli stereodescrittori sin/anti
Sin = se il sostituente è orientato verso l'anello a più bassa numerazione
Anti = se il sostituente è orientato dalla parte opposta
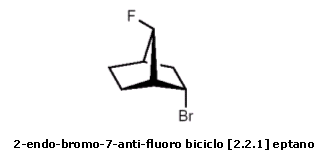
Il carbonio tetraedrico è il più diffuso, ma non l'unico stereocentro possibile. Altri atomi ed altre geometrie, oltre a quella tetraedrica, sono in grado di costituire strutture stereogeniche
In generale, qualunque disposizione spaziale stabile di atomi priva di elementi di simmetria riflessiva è compatibile con l'esistenza di molecole chirali e quindi di enantiomeri. Tra i centri stereogenici più importanti oltre al Carbonio vi sono l'Azoto, il Fosforo, lo Zolfo, il Silicio e molti metalli di transizione (composti di coordinazione o complessi chirali).
Azoto stereogenico
L'azoto forma molecole chirali quando è legato a tre sostituenti diversi. In questa forma presenta una geometria piramidale trigonale con un doppietto elettronico non condiviso. Il doppietto elettronico viene considerato come quarto sostituente e ad esso viene assegnata la priorità CIP più bassa.
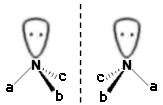
Un esempio di composti chirali di questo tipo sono le ammine terziarie.
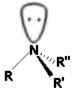
Tuttavia le ammine terziarie, pur essendo chirali, non manifestano attività ottica. Ciò è dovuto al fatto che i due enantiomeri sono in reciproco equilibrio, potendosi convertire l'uno nell'altro. La configurazione subisce infatti una rapida inversione attraverso uno stato di transizione trigonale planare.
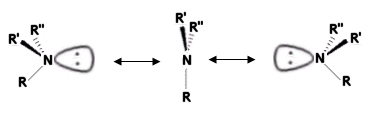
Nell'ammoniaca l'inversione avviene con una frequenza di 2 x 1011 Hz. Nelle ammine terziarie, dove i tre sostituenti sono più ingombranti rispetto ai tre atomi di idrogeno dell'ammoniaca, l'inversione avviene più lentamente, ma comunque ad una velocità tale da non permettere, a temperatura ambiente, la separazione dei due enantiomeri.
Se l'azoto viene sostituito con atomi di maggior dimensione, come il Fosforo o lo Zolfo, la struttura piramidale si inverte più lentamente e con maggior difficoltà e possono così essere isolati enantiomeri otticamente attivi.
L'Azoto può tuttavia generare enantiomeri isolabili e quindi otticamente attivi quando la transizione tra le due forme enantiomeriche viene impedita. Ciò può ad esempio accadere quando l'azoto fa parte di composti ciclici (aziridine, base di Troger) o quando condivide il suo doppietto elettronico con altri atomi (ioni ammonio, N-ossidi)
Nelle Aziridine l'Azoto fa parte di un anello triangolare che ne impedisce l'inversione. Si vedano, ad esempio, i due enantiomeri della 1-cloro-2,2-difenilaziridina (Ph = gruppo fenile)
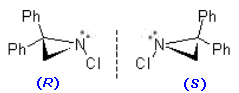
Altri esempi di ammine in configurazioni chirali stabili sono i composti ciclici fusi a ponte con l'azoto in posizione di 'ponte' o in posizione 'testa di ponte'. La rigidità di queste strutture impedisce l'inversione dell'azoto. Vengono chiamati 'fusi a ponte' i sistemi ciclici con più di due atomi in comune,.
Un tipico esempio è la base di Troger, dove sono presenti due atomi di azoto stereogenici in posizione testa di ponte.
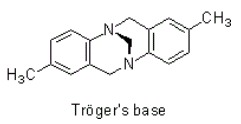
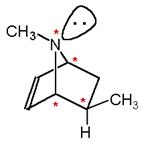
Si veda infine, la seguente ammina terziaria biciclica in cui l'azoto forma un ponte tra i due anelli fusi. Si notino i 4 stereocentri indicati con gli asterischi. Si noti inoltre che senza il gruppo metile in posizione 'eso' la molecola presenterebbe un piano di simmetria e sarebbe pertanto un composto meso.
Nei Sali di tetraalchilammonio e negli N-ossidi l'Azoto utilizza il suo doppietto libero per legare un quarto gruppo. Anche in questo caso l'inversione non è possibile è possono quindi essere isolati gli enantiomeri.
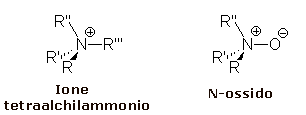
Fosforo stereogenico
Il fosforo appartiene allo stesso gruppo chimico dell'azoto (V A). Può formare sia composti fosforganici chirali tricoordinati e tetracoordinati, come l'azoto, che pentacoordinati.
I composti del fosforo tricoordinati, analoghi alle ammine terziarie, sono le fosfine ( o fasfani).
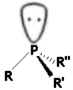
A differenza delle ammine terziarie che presentano una barriera energetica per l'inversione dell'ordine dei 25-40 kJ/mol, le fosfine hanno un'energia di inversione di 120-140 kJ/mol. A temperatura ambiente la barriera energetica è sufficientemente elevata da non consentire una rapida inversione tra le forme enantiomeriche delle fosfine, permettendo così la loro separazione. Si consideri ad esempio la fenil-metil-propil-fosfina
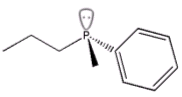
Assegniamo la configurazione assoluta
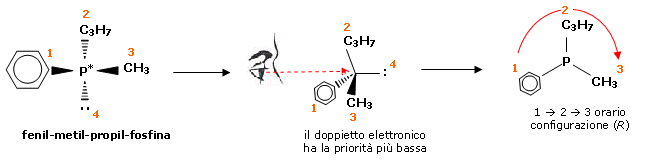
I due enantiomeri sono allora:
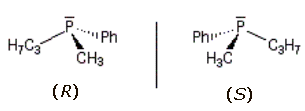
(Ph = gruppo fenile)
Anche il Fosforo, come l'Azoto, presenta composti chirali tetracoordinati a struttura tetraedrica
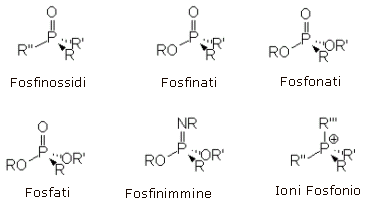
Il fosforo è in grado di formare anche composti chirali pentacoordinati con struttura bipiramidale trigonale del tipo
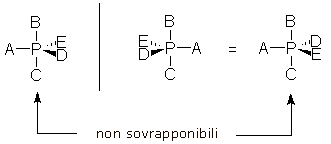
Zolfo stereogenico
Lo zolfo può formare composti solforganici chirali
trivalenti (piramidali) e tetravalenti (tetraedrici)
I composti trivalenti sono chirali
quando lo zolfo è legato a tre gruppi differenti con il doppietto elettronico
che funge da quarto sostituente a più bassa priorità. Sono composti di questo
tipo i Solfossidi, i Solfiti, gli ioni Solfonio, i Solfinati (o esteri
solfinici).
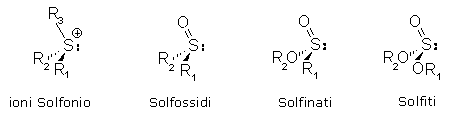
I composti tetravalenti sono chirali quando lo Zolfo è legato a quattro sostituenti diversi.
I solfossidi presentano una barriera di inversione piuttosto elevata, compresa tra i 145 e i 185 kJ/mol. Le loro miscele racemiche possono quindi essere risolte nei singoli enantiomeri anche a temperatura ambiente.
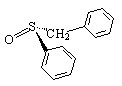
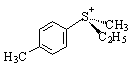
(R)-Solfossido [![]() ]D
= +92.4° (R)-Solfonio [
]D
= +92.4° (R)-Solfonio [![]() ]D
= -15.8°
]D
= -15.8°
Silicio stereogenico
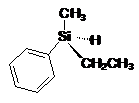 Il
Silicio, come il Carbonio, forma composti chirali quando è legato a quattro
gruppi diversi in struttura tetraedrica.
Il
Silicio, come il Carbonio, forma composti chirali quando è legato a quattro
gruppi diversi in struttura tetraedrica.
Sono possibili stereocentri privi di atomi si vedano, ad esempio, i due enantiomeri di un adamantano tetrasostituito. In questo caso lo stereocentro è localizzato al centro della gabbia molecolare
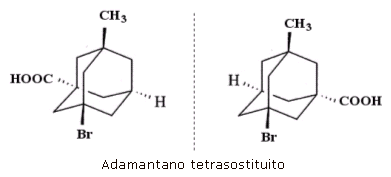
Stereocentri non tetraedrici
Come abbiamo già detto i più importanti esempi di stereocentri non tetraedrici si presentano nei composti di coordinazione o complessi, una famiglia di composti che presenta molti altri tipi di isomerie e che tratteremo pertanto in un capitolo successivo
La chiralità può essere dovuta ad una configurazione avvitata (elicoiale) della molecola. Le molecole di questo tipo possono presentarsi in due forme enantiomeriche, distinguibili in relazione al senso di avvitamento destrorso o sinistrorso. Per distinguerle si usano gli stereodescrittori P/M (Plus/Minus). Se l'enantiomero presenta un avvitamento destrorso si assegna la configurazione P, se presenta un avvitamento sinistrorso si assegna la configurazione M. Un esempio classico è dato dall'Elicene.
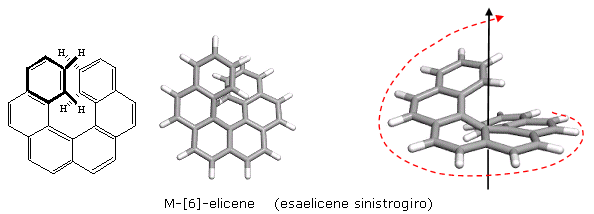
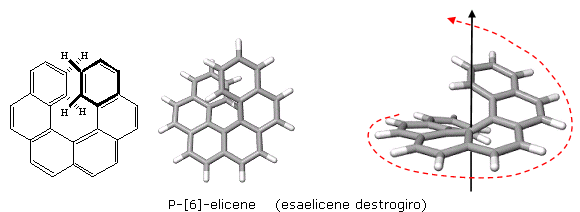
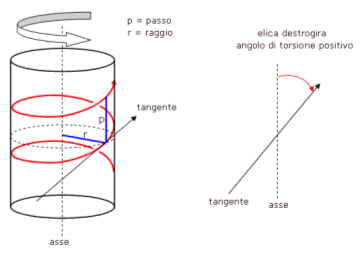
La simmetria elicoidale può essere definita attraverso l'individuazione di due rette sghembe (non appartenenti al medesimo piano) tra loro non perpendicolari. Tali rette possiedono una, ed una sola, perpendicolare in comune. In questo modo è possibile definire un sistema elicoidale in cui una retta funge da asse di un avvolgimento elicoidale all'interno di un cilindro, mentre la seconda retta risulta tangente al cilindro e permette di definire il raggio, il passo ed il senso di avvitamento.
Il raggio dell'elica è la distanza delle due rette misurata lungo la perpendicolare comune.
Il passo dell'elica è la distanza tra due spire misurata sulla superficie laterale del cilindro lungo una retta parallela all'asse dell'elica
Il senso di avvolgimento è definito dall'angolo individuato dalle proiezioni delle due rette su di un piano (angolo di torsione). Se l'angolo che la retta più vicina all'osservatore forma con quella più distante è positivo (la retta più vicina è ruotata in senso orario), l'avvolgimento è destrorso, altrimenti è sinistrorso.
La molecola non deve necessariamente possedere almeno una spira completa per presentare una chiralità elicoidale (vedi l'esempio seguente).
1° Esempio - Propeller
Le molecole propeller (propulsore, elica) possono essere considerate come un caso più generale rispetto ai bifenili a rotazione impedita (che vedremo come esempio di chiralità assiale). Sono costituite da 3 o più strutture planari rigide collegate ad un atomo centrale, con sostituenti ingombranti che ne impediscono la libera rotazione.
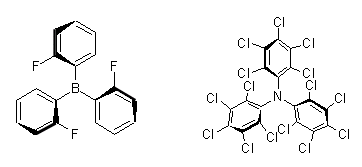
2° Esempio - Twistano
Il twistano è un triciclodecano formato da anelli fusi di cicloesano in conformazione a treccia (twist)
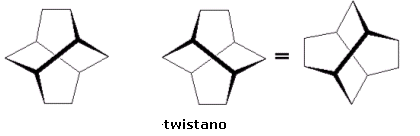
La chiralità assiale si genera quando due coppie di sostituenti, ciascuno diverso dall'altro all'interno di una medesima coppia, si trovano legate alle due estremità di una struttura molecolare rigida allungata (asse stereogenico o, impropriamente, asse chirale), in modo da presentarsi sfalsati, se osservati lungo l'asse stereogenico.
E' possibile immaginare un asse stereogenico come il risultato di uno stiramento di un centro stereogenico tetraedrico
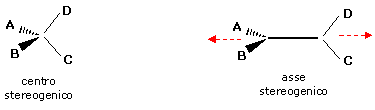
Mentre un centro stereogenico tetraedrico per generare un composto chirale deve possedere 4 sostituenti diversi (a b c d), un asse stereogenico per generare un composto chirale deve presentare i due sostituenti di ogni coppia diversi tra loro. Risultano pertanto chirali anche i composti del tipo
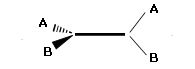
La configurazione assoluta di un enantiomero che presenta chiralità assiale viene definita in modo analogo a quanto già visto per la chiralità centrale, utilizzando le regole CIP per assegnare la priorità ai quattro sostituenti.
Si osserva l'enantiomero lungo l'asse stereogenico in modo che due sostituenti risultino più vicini all'osservatore e due più distanti. Si assegna la priorità prima ai sostituenti più vicini, i quali presenteranno pertanto sempre priorità 1 e 2. Poi si assegna la priorità ai sostituenti più distanti, i quali presenteranno quindi sempre priorità 3 e 4. (Nella chiralità assiale i sostituenti anteriori hanno sempre priorità maggiore rispetto a quelli posteriori).
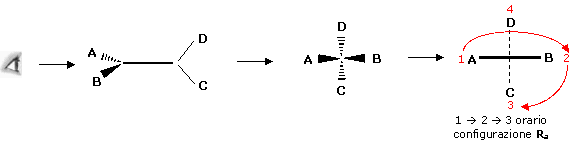 Si osserva poi il movimento 1 3
(anche in questo caso il sostituente a minor priorità viene trascurato). Se il
movimento è orario si assegna la configurazione Ra, se è
antiorario si assegna la configurazione Sa
(la lettera 'a' a pedice degli stereodescrittori R/S sta ovviamente per 'assiale')
Si osserva poi il movimento 1 3
(anche in questo caso il sostituente a minor priorità viene trascurato). Se il
movimento è orario si assegna la configurazione Ra, se è
antiorario si assegna la configurazione Sa
(la lettera 'a' a pedice degli stereodescrittori R/S sta ovviamente per 'assiale')
Un composto che presenta chiralità assiale può essere classificato anche usando gli stereodescrittori P/M (Plus/Minus) della chiralità elicoidale. E' infatti possibile immaginare che la coppia dei sostituenti che si trova ad una estremità dell'asse stereogenico abbia subito una torsione, un avvitamento rispetto alla coppia che si trova all'altra estremità. Per definire il senso di questo avvitamento è necessario congiungere idealmente con due segmenti i sostituenti ad analoga priorità che si trovano alle estremità dell'asse stereogenico. Quindi il sostituente a maggior priorità anteriore con il sostituente a maggior priorità posteriore (1 - 3) ed il sostituente a minor priorità anteriore con il sostituente a minor priorità posteriore (2 - 4) ed osservare, lungo l'asse stereogenico, l'angolo di torsione. Se l'angolo di torsione è positivo (segmento 2-4 ruotato in senso orario rispetto a segmento 1- 3) il composto è P. Se l'angolo di torsione è negativo (segmento 2-4 ruotato in senso antiorario rispetto a segmento 1- 3) il composto e M.
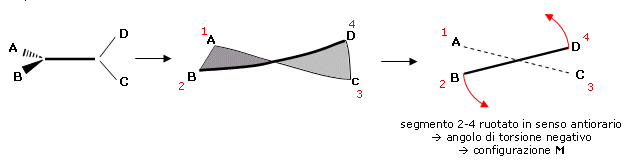
Per maggior semplicità è sufficiente osservare il composto lungo l'asse stereogenico. Se il movimento 1 3, che porta il sostituente a maggior priorità anteriore (1) verso il sostituente a maggior priorità posteriore (3), è orario il composto è P, se è antiorario è M.
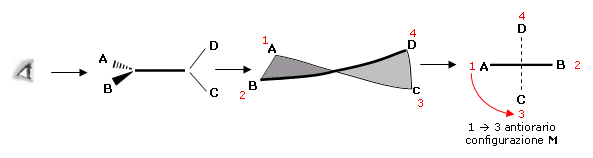
In definitiva esiste la seguente corrispondenza tra gli stereodescrittori della chiralità assiale ed elicoidale: Ra = M ed Sa = P
Esempi di chiralità assiale
1° esempio - alleni
Gli alleni sono dei dieni cumulati che presentano pertanto due doppi legami adiacenti separati da un carbonio ibridato sp. L'asse stereogenico è costituito dal gruppo C=C=C. Ciascun doppio legame giace su di un piano perpendicolare rispetto all'altro formando una struttura lineare rigida che costringe i sostituenti alle due estremità dell'asse stereogenico ad assumere una conformazione sfalsata stabile. Gli alleni sono chirali solo se i due sostituenti che formano ciascuna coppia sono tra loro diversi. Se nella molecola sono presenti più assi stereogenici (più doppi legami cumulati) l'allene può essere chirale solo se possiede un numero dispari di doppi legami cumulati.
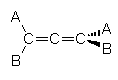

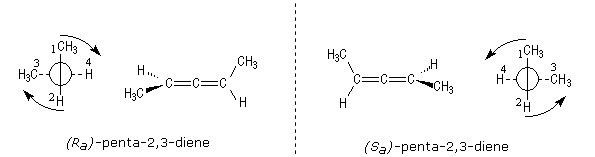
Si noti che ai fini della assegnazione della configurazione assoluta all'enantiomero è indifferente porre il punto di osservazione in corrispondenza dell'una o dell'altra estremità dell'asse stereogenico.
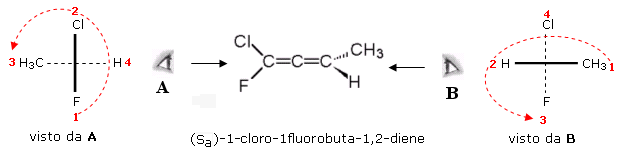
2° esempio - Alchilidencicloalcani
Negli alchilidencicloalcani l'asse stereogenico è costituito da un doppio legame C=C saldato ad un cicloalcano
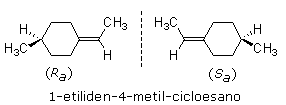
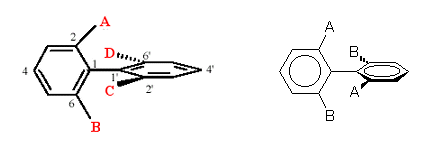
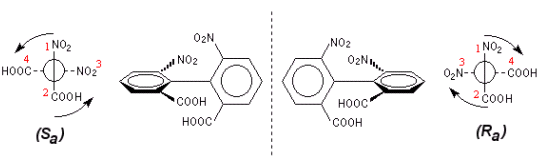
3° esempio - Bifenili
I bifenili sono formati da due anelli benzenici uniti da un legame semplice. Se ciascun anello presenta dei sostituenti in posizione orto (posizioni 2,6 e 2',6') sufficientemente voluminosi, l'ingombro sterico impedisce la libera rotazione degli anelli benzenici attorno al legame semplice che li unisce. Se i due sostituenti di ciascun anello benzenico sono tra loro differenti si formano due enantiomeri, detti atropisomeri.
L'atropisomeria è una particolare forma di enantiomeria che si manifesta quando due conformeri sono separati da un'energia rotazionale sufficientemente elevata da impedirne la rapida reciproca interconversione ed i due conformeri sono uno l'immagine non sovrapponibile dell'altro. A causa dell'elevata barriera energetica gli atropisomeri sono isolabili. La risolvibilità della miscela racemica dipende ovviamente dall'ingombro sterico dei sostituenti.
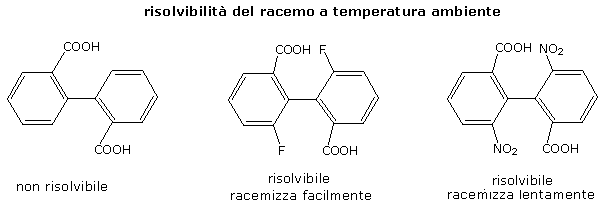
Nei bifenili l'asse stereogenico coincide con il legame semplice che tiene uniti i due anelli benzenici (direzione 1-1')
![]()
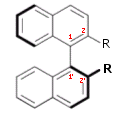
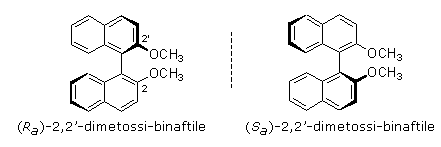
4° esempio - Binaftili
I binaftili sono formati da due anelli biciclici naftalenici uniti da un legame semplice (posizione 1-1'). Se ciascuna anello biciclico presenta un sostituente in posizione 2, sufficientemente voluminoso, l'ingombro sterico impedisce la libera rotazione degli anelli attorno al legame semplice che li unisce. In modo analogo a quel che accade nei bifenili, i due enantiomeri che si formano sono atropisomeri.
5° esempio - Spirani
Gli spirani sono costituiti da due anelli aventi in comune un solo atomo di carbonio ibridato sp3. Ne consegue che i due anelli non possono essere complanari, ma giacciono su due piani tra loro perpendicolari.
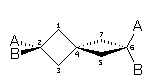
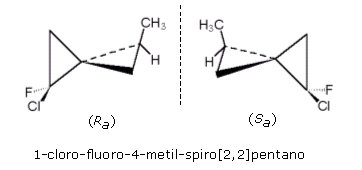
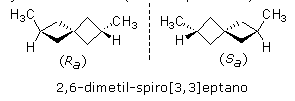
6° esempio - Adamantani
L'adamantano è un decano triciclico saturo avente la seguente struttura
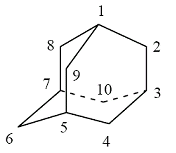
Gli adamantani disostituiti in posizioni 2,6 (o equivalenti) danno luogo ad una chiralità assiale con l'asse stereogenico passante per i due atomi di carbonio sostituiti.
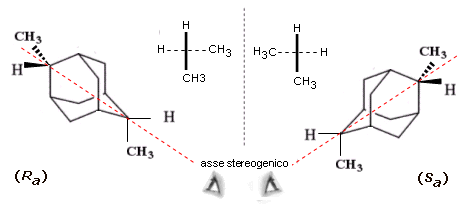
La chiralità planare si genera quando un gruppo di atomi disposti su di un piano (piano stereogenico o, impropriamente, piano chirale) sono connessi ad una struttura rigida (spesso a ponte) che si estende sopra o sotto il piano.
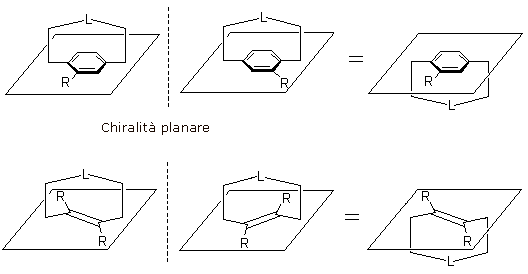
La configurazione assoluta di un enantiomero che presenta chiralità planare viene definita utilizzando gli stereodescrittori Rp/Sp, dove la lettera 'p' a pedice degli stereodescrittori R/S sta ovviamente per 'planare'.
L'assegnazione della configurazione assoluta di un enantiomero che presenta chiralità planare prevede i seguenti passaggi:
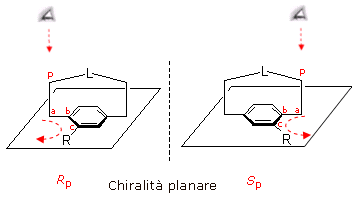
Anche la chiralità planare può essere classificata con gli stereodescrittori P/M (Plus/Minus) della chiralità elicoidale. Per farlo è necessario osservare la successione di atomi P-a-b-c lungo l'asse che congiunge i due atomi centrali a-b. Se l'angolo diedro che separa il piano Pab dal piano abc è positivo l'enantiomero avrà configurazione P, se è negativo avrà configurazione M.
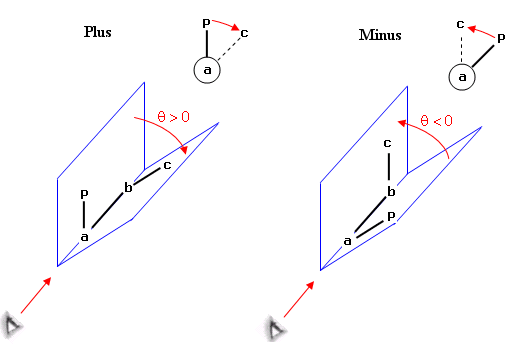
Nella chiralità planare è sempre vera l'eguaglianza Rp = P ed Sp = M.
Si ricordi che nella chiralità assiale invece Ra = M ed Sa = P
1° Esempio - composti ad ansa
I composti ad ansa presentano in genere un anello insaturo planare, che definisce il piano stereogenico, al quale è collegata una catena ciclica satura troppo breve per permettere la libera rotazione del gruppo planare.
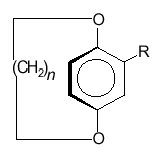
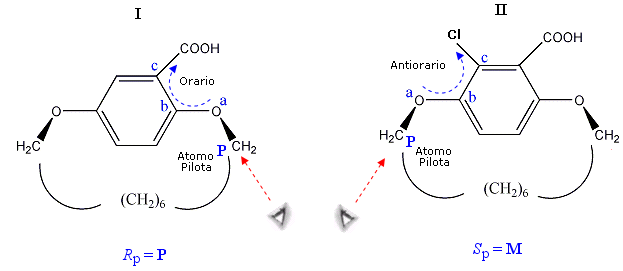
Nel caso dei due composti successivi (I e II), ad esempio, il piano stereogenico è costituito dall'anello benzenico e dai suoi sostituenti (i due atomi di ossigeno, il carbossile ed il cloro nel composto II). L'ansa è costituita da una catena satura di 8 atomi di carbonio. Al piano stereogenico sono legati, tramite i due atomi di ossigeno, due atomi di carbonio che potrebbe fungere da Atomo Pilota. Tra i due si seleziona quello a maggior priorità. Per il composto I l'atomo pilota (a maggior priorità) è quello più vicino al carbossile. Nel caso del composto II l'atomo pilota (a maggior priorità) è quello più vicino al cloro (che ha priorità maggiore del carbonio carbossilico). I primi due atomi (a, b) del percorso sul piano stereogenico sono obbligati. Il terzo (c) è l'atomo di carbonio a maggior priorità tra i due adiacenti all'atomo b.
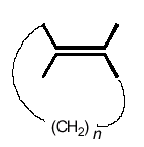
2° Esempio - Cicloalcheni
I cicloalcheni sono composti anulari con un doppio legame che individua il piano stereogenico. Analogamente ai composti ad ansa, se l'anello alifatico saturo (CH2)n è abbastanza breve il piano stereogenico non può ruotare liberamente
Nel trans-cicloottene (o (E)-cicloottene) vi sono due atomi legati alle due estremità del piano stereogenico che, presentando la medesima priorità, possono indifferentemente essere scelti come 'atomo pilota'. Come si osserva nell'immagine successiva, la diversa scelta non influisce sull'attribuzione della configurazione.
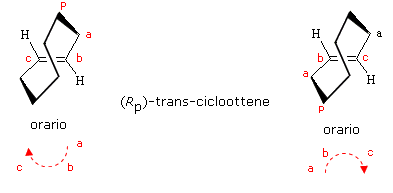
Nel caso invece di un cicloottene sostituito la scelta dell'atomo pilota diventa obbligata. Si noti come, sostituendo un idrogeno con un atomo di fluoro la configurazione passi da E a Z.
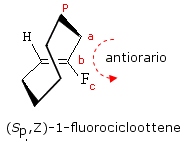
3° Esempio - Paraciclofani
I paraciclofani sono costituiti da due anelli benzenici saldati, in posizione para, da due catene alifatiche
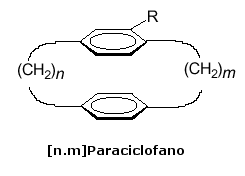
Nel caso di un unico sostituente su di un anello benzenico l'attribuzione della configurazione risulta semplice
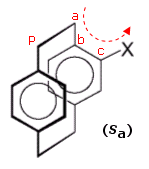
Nel caso di più sostituenti su più anelli l'attribuzione può dar luogo ad ambiguità. Si veda l'esempio successivo in cui ciascuno dei due anelli benzenici costituisce un piano stereogenico (in primo piano a, in secondo piano b).
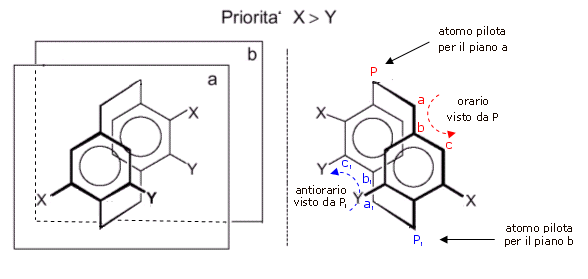
4° Esempio - Annuleni a ponte
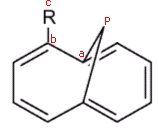
5° Esempio - Metalloceni bisostituiti
I metalloceni sono costituiti da due anelli ciclopentadienilici disposti parallelamente legati ad un atomo metallico disposto tra di essi.
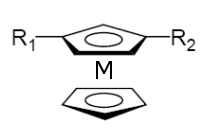
Il ferrocene disostituito in posizioni 1,2 e 1,3, ad esempio, manifesta chiralità planare. Per assegnare la configurazione ci si pone sopra il piano stereogenico, dalla parte opposta dell'atomo metallico e si osserva il movimento dal sostituente a maggior priorità verso quello a minor priorità. Se il movimento è orario si assegna la configurazione Rp, se è antiorario si assegna la configurazione Sp.
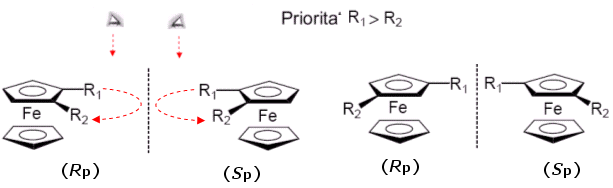
Con molecole più complesse (più di due sostituenti) l'attribuzione della configurazione può dar luogo a situazioni ambigue. Si preferisce allora assegnare a ciascun atomo di carbonio legato ad un sostituente gli stereodescrittori R/S della chiralità centrale, trattandolo come un atomo di carbonio tetraedrico. Per far ciò si assume che l'atomo metallico formi, con tutti gli atomi di carbonio che costituiscono l'anello pentadienilico, altrettanti legami semplici.
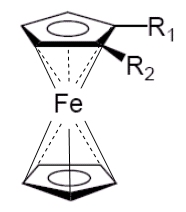
Si prenda ad esempio l'acido 2-metilferrocene 1-carbossilico. Avendo il carbonio carbossilico priorità maggiore rispetto al carbonio metilico, l'enantiomero avrà chiralità planare (Rp)
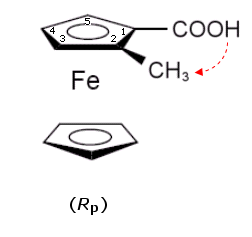
E' tuttavia possibile considerare i due atomi di carbonio C1 e C2 come tetraedrici ed assegnar loro gli stereodescrittori R/S della chiralità centrale. Per il carbonio C2, ad esempio, si trova che i suoi quattro sostituenti presentano il seguente ordine di priorità CIP: Fe > C1 > C3 > CH3
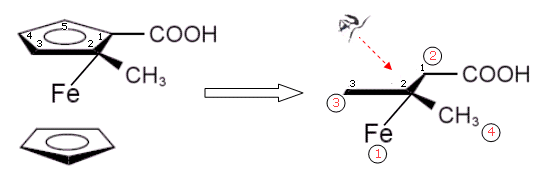
Osservando quindi il carbonio C2 in modo da avere il sostituente a minor priorità in posizione opposta all'osservatore, gli si assegna la configurazione assoluta
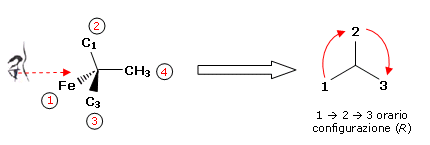
Eseguendo la medesima operazione anche per il carbonio C1, si trova che presenta configurazione (S) e quindi l'enantiomero è l'acido (1S,2R)-2-metilferrocene 1-carbossilico
 |
|
| Appunti Geografia |  |
| Tesine Ingegneria tecnico |  |
| Lezioni Biologia |  |