 |
|
| Appunti scientifiche |
|
 |
|
| Appunti scientifiche |
|
| Visite: 15170 | Gradito: |
Leggi anche appunti:L'industria chimicaL'INDUSTRIA CHIMICA L'industria chimica prevede, partendo da materiali che La distribuzione degli elettroni negli atomiLA DISTRIBUZIONE DEGLI ELETTRONI NEGLI ATOMI Un atomo si trasforma in ione Gli anni '20 [del novecento] - ricerca atomicaGLI ANNI '20 [DEL NOVECENTO] - RICERCA ATOMICA 1 I CENTRI DELLA RICERCA ATOMICA |
 |
 |
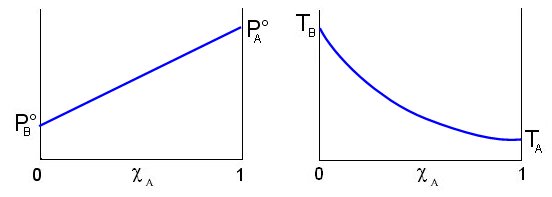
Per descrivere il processo di distillazione si fa riferimento alla curva che lega la temperatura di ebollizione della soluzione alla frazione molare del componente più volatile. Il componente più volatile è ovviamente quello con la più alta tensione di vapore e quindi con la più bassa temperatura di ebollizione. TB è la temperatura di ebollizione del componente B puro e TA è la temperatura di ebollizione del componente A puro.
Come si può osservare nei grafici successivi, a differenza della tensione di vapore, la temperatura di ebollizione della soluzione non varia linearmente in funzione di cA
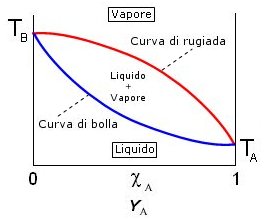
Se in ascissa si riporta sia la frazione molare della soluzione (c) che del vapore (Y) si ottengono due curve a pressione costante (isobare) che costituiscono il cosiddetto diagramma lenticolare. La curva inferiore, che rappresenta la temperatura alla quale il liquido bolle, è detta curva di bolla. La curva superiore, che rappresenta la temperatura alla quale il vapore condensa, è detta curva di rugiada. All'interno della lente è presente un sistema bifasico liquido + vapore in reciproco equilibrio
Come abbiamo già detto la distillazione permette di separare i due componenti a diversa volatilità di una soluzione sfruttando il fatto che il vapore risulta più ricco nel componente più volatile. Facendo ricondensare i vapori, la nuova soluzione che se ne ottiene risulta anch'essa più concentrata nell'elemento più volatile. Eseguendo più volte il processo è possibile separare completamente i due componenti.
|
|
Distillazione Portiamo alla temperatura di ebollizione T1 un liquido povero (c ) nel componente più volatile A, ottenendo in tal modo un vapore più ricco (y2 > c ) nel componente più volatile A. Condensiamo il vapore, ottenendo un liquido avente la medesima concentrazione in A (c = y2) del vapore Portiamo nuovamente alla temperatura di ebollizione T2 il liquido raccolto, ottenendo in tal modo un vapore ancor più ricco (y3 > c ) nel componente più volatile A. Condensiamo di nuovo il vapore, ottenendo un liquido avente la medesima concentrazione in A (c = y3) del vapore |
Si tenga presente che la regola della leva può essere applicata anche ai diagrammi isobari lenticolari ed in generale a qualsiasi sistema bifasico in equilibrio, ad esempio una lega metallica solida in equilibrio con il suo fuso.
|
Esempio Consideriamo una lega Nichel-Rame contenente il 53% in massa di Nichel. Il Nichel puro fonde a 1453 °C, mentre il Rame puro fonde a 1085°C. A 1300°C si forma un sistema bifasico con il solido in equilibrio con il suo fuso. Nel diagramma lenticolare a destra vediamo che l'isoterma di 1300 °C incontra la curva di Liquidus (curva rossa = temperatura di solidificazione del liquido in funzione della % in massa del Nichel nel liquido) in corrispondenza di una concentrazione in massa di Nichel pari al 45%, mentre incontra la curva di Solidus (curva blu = temperatura di fusione del solido in funzione della % in massa del Nichel nel solido) in corrispondenza di una concentrazione in massa di Nichel pari al 58%. In altre parole, quando una lega metallica fonde genera un fuso più ricco nel componente a minor punto di fusione (Rame) e quindi più povero nel componente a maggior punto di fusione (Nichel). Ovviamente il solido residuo in equilibrio con il fuso risulta più ricco nel componente a maggior punto di fusione (Nichel). La percentuale in massa della fase liquida si ottiene con la regola della leva
a 1300 °C il sistema bifasico è dunque costituito dal 38,5% in massa di fuso (più concentrato in rame) e dal 61.5% in massa di solido (più ricco di Nichel) |
|
 |
|
| Appunti Geografia |  |
| Tesine Biologia |  |
| Lezioni Ingegneria tecnico |  |