 |
|
| Appunti scientifiche |
|
 |
|
| Appunti scientifiche |
|
| Visite: 2504 | Gradito: |
Leggi anche appunti:Coefficienti stechiometrici e bilanciamentoCoefficienti stechiometrici e bilanciamento Affinché l'equazione descriva Gli EnzimiGli Enzimi Caratteristiche generali: sono proteine: struttura terziaria Calcolo del pH di acidi e basi deboli molto diluiti e/o molto deboliCalcolo del pH di acidi e basi deboli molto diluiti e/o molto deboli Quando |
 |
 |
È infine possibile combinare l'equazione di Clausius-Clapeyron con la Legge di Raoult per soluti poco volatili ed ottenere una dipendenza dei DT crioscopici ed ebullioscopici dalla concentrazione.
Se infatti consideriamo la tensione di vapore di una soluzione che contenga un soluto poco volatile e la tensione di vapore del solvente puro in relazione alle rispettive temperature di solidificazione, possiamo scrivere
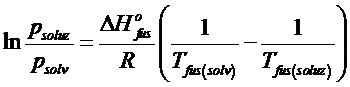
dove compare l'entalpia di fusione (DH°fus = calore latente del passaggio di stato).
Ricordando che per la legge di Roult, essendo il soluto poco volatile (psoluto ≈ 0), avremo
![]()
e dunque
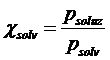
L'equazione di Clausius-Clapeyron diventa
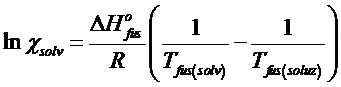
Esempio
33,07 g di saccarosio sono disciolti in 85,27 g di acqua. La soluzione congela a -2,02°C. Calcolare il Peso molare del saccarosio, sapendo che l'entalpia di fusione dell'acqua è 6,01 kJ mol-1
Sapendo che l'acqua congela a 273,15K e che la soluzione di saccarosio congela a 273,15-2,02=271,13K, possiamo calcolare la frazione molare del solvente
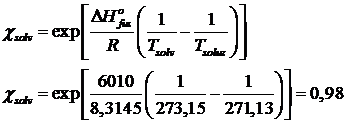
e dunque
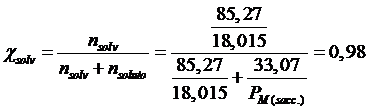
da cui PM(sacc) = 342 g mol-1
* * * * * * *
Introducendo alcune approssimazioni è possibile utilizzare l'equazione di Clausius-Clapeyron per stimare la costante crioscopica. Riscriviamo la relazione come
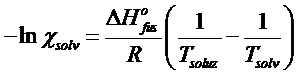
prima approssimazione
Se la soluzione è diluita (la legge di Raoult è valida per soluzioni ideali e quindi diluite) si avrà
csolv e csoluto
e quindi potremo scrivere
![]()
In soluzioni diluite è possibile approssimare il logaritmo della frazione molare del solvente con la frazione molare del soluto
Seconda approssimazione
Se la variazione del punto di congelamento è piccola possiamo porre
![]()
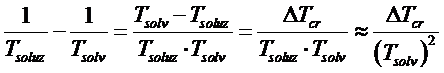
Applicando le due approssimazioni la relazione diventa
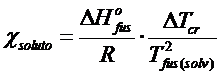
che, riordinata, fornisce
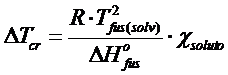
Terza approssimazione
Se la soluzione è diluita possiamo scrivere
nsolv + nsoluto ≈ nsolv
e quindi
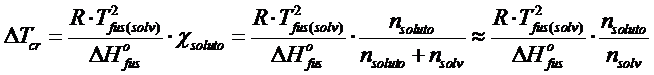
Se ora moltiplichiamo e dividiamo il secondo membro per il peso molare del solvente espresso in kg mol-1, otteniamo
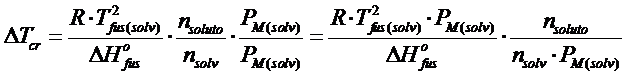
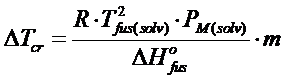
dove m è la molalità della soluzione
Se confrontiamo questa ultima relazione con
![]()
si trova che
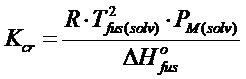
Esempio
Calcolare la costante crioscopica molale dell'etanolo (PM = 46,07 g mol-1) sapendo che la sua entalpia standard di fusione è ΔH°fus = 4,9 kJ mol-1 e la temperatura di fusione è pari a 158,8K
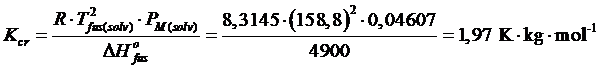
* * * * * *
Ovviamente le medesime relazioni si possono ottenere in modo del tutto analogo anche per l'innalzamento ebullioscopico
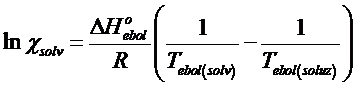
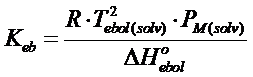
Esempio
Stimare l'entalpia standard di ebollizione (evaporazione) dell'acetone (PM =58,08 g mol-1), sapendo che la sua temperatura normale di ebollizione vale 329,4K e la sua costante ebullioscopia molale è pari a Keb = 1,7 K·kg·mol-1
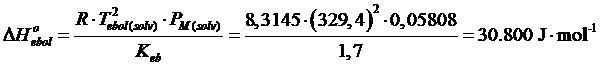
 |
| Appunti su: equazione di clausius clapeyron, equazione di Clapeyron, Legge di Clausius Clapeyron, https:wwwappuntimaniacomscientifichechimicaequazione-di-clausiusclapeyron44php, |
|
| Appunti Geografia |  |
| Tesine Ingegneria tecnico |  |
| Lezioni Biologia |  |