 |
|
| Appunti scientifiche |
|
 |
|
| Appunti scientifiche |
|
| Visite: 4364 | Gradito: |
Leggi anche appunti:Il Processo DryIl Processo Dry Il primo processo di realizzazione della doppia giunzione Composti e legami ioniciComposti e legami ionici 1 Le soluzioni che contengono ioni conducono la corrente Relazione di agenti inquinanti - determinazione della durezza totale dell'acquaRelazione di agenti inquinanti Titolo : determinazione della durezza totale |
 |
 |
Il gruppo carbossilico
Gli alcoli sono composti caratterizzati dal gruppo funzionale ossidrile (-OH), mentre gli acidi carbossilici sono composti caratterizzati dal gruppo funzionale carbossile (-COOH)
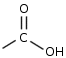
Gli acidi carbossilici sono più acidi degli alcoli. In soluzione acquosa un acido carbossilico di dissocia in un anione carbossilato (RCOO-) ed un idrogenione (H+).
RCOOH → RCOO- + H+
La maggior acidità di un acido carbossilico rispetto ad un alcol è legata al fatto che l'anione carbossilato, che si forma dalla dissociazione ionica dell'acido, è più stabile dell'anione alcossido (RO-), che si forma dalla dissociazione ionica di un alcol.
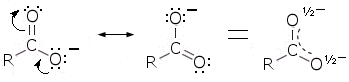
L'anione carbossilato viene stabilizzato principalmente per effetto di risonanza.
L'effetto risonante è dovuto alla sovrapposizione dell'orbitale p dell'Ossigeno che porta la carica negativa con il legame π del gruppo carbonilico (sistema coniugato π-p). Come conseguenza della risonanza la carica negativa è dispersa e portata equamente dai due atomi di ossigeno. Il gruppo carbossilico risulta quindi planare, con il carbonio ed i due atomi di ossigeno ibridati sp2.
il gruppo peptidico
Gli amminoacidi che costituiscono le proteine presentano la seguente struttura generale
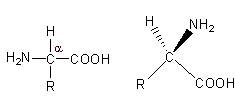
Un carbonio centrale tetraedrico (detto carbonio alfa) al quale è legato un gruppo amminico (-NH2) di natura basica, un gruppo carbossilico (-COOH) di natura acida, un atomo di idrogeno ed un gruppo chimico (-R), detto residuo aminoacidico o gruppo R, diverso da amminoacido ad amminoacido.
Gli amminoacidi si legano tra loro a formare le proteine tramite un legame di condensazione, facendo reagire il gruppo amminico di un amminoacido con il gruppo carbossilico di un altro, con perdita di una molecola di acqua.
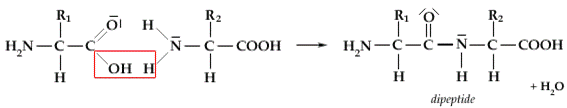
Il legame che si produce è detto legame peptidico ed il gruppo chimico CONH è detto gruppo peptidico.
![]()
gruppo peptidico
In questo modo tutte le proteine si presentano costituite da un lungo filamento chimico comune, formato dalla successione di gruppi CH e CONH, dal quale sporgono i residui aminoacidici (-R), la cui successione è diversa da proteina a proteina.
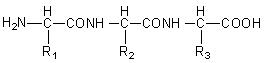
I filamenti proteici non rimangono mai lineari. Rispondendo alle sollecitazioni prodotte dalle loro polarità interne si ripiegano su se stessi formando strutture a diverso grado di complessità che risultano fondamentali nel determinare la funzione proteica.
Il primo livello di ripiegamento proteico (struttura secondaria) si produce grazie alla possibilità di rotazione dei gruppi CH rispetto ai gruppi peptidici (CONH) lungo tutto il filamento.
La rotazione è invece impedita lungo il legame peptidico C-N che presenta un parziale carattere di doppio legame a causa di un fenomeno di risonanza. L'effetto risonante è dovuto alla sovrapposizione dell'orbitale p dell'Azoto che porta un doppietto solitario con il legame π del gruppo carbonilico (sistema coniugato π-p).
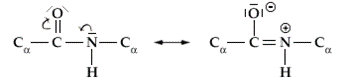
Come conseguenza della risonanza gli atomi del gruppo peptidico (CONH) giacciono tutti su di un medesimo piano. Questi piani rigidi possono ruotare rispetto al carbonio-alfa. In questo modo, ogni piano delle unità peptidiche ha due rotazioni possibili: una intorno al legame tra il carbonio-alfa e l'atomo di azoto del gruppo peptidico C-N (angolo di rotazione Φ, fi), l'altra intorno al legame tra l'atomo di carbonio-alfa e l'atomo di carbonio del gruppo peptidico C-C' (angolo di rotazione ψ, psi).
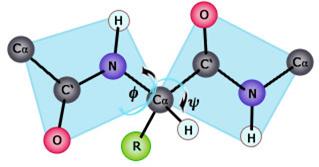
Tali rotazioni permettono al filamento proteico di avvolgersi su se stesso secondo schemi diversi, raggiungendo una struttura finale stabile.
 |
| Appunti su: gruppi carbossilico analisi TGA, |
|
| Appunti Biologia |  |
| Tesine Geografia |  |
| Lezioni Ingegneria tecnico |  |